Багато компаній та виробів XX століття виглядали настільки непорушно на ринку, що неможливо було уявити їхню відсутність в недалекому майбутньому. Проте, інновації здатні залишити будь-який бізнес у минулому, якщо він не зможе пристосуватися до сучасних реалій, нових технологій роботи, потреб клієнта в нових продуктах та властивостях цих продуктів.
В хімії води показники рН*, загальної жорсткості**, лужності*** та кількості вуглекислоти**** контролюють усі процеси корозії та накипоутворення.
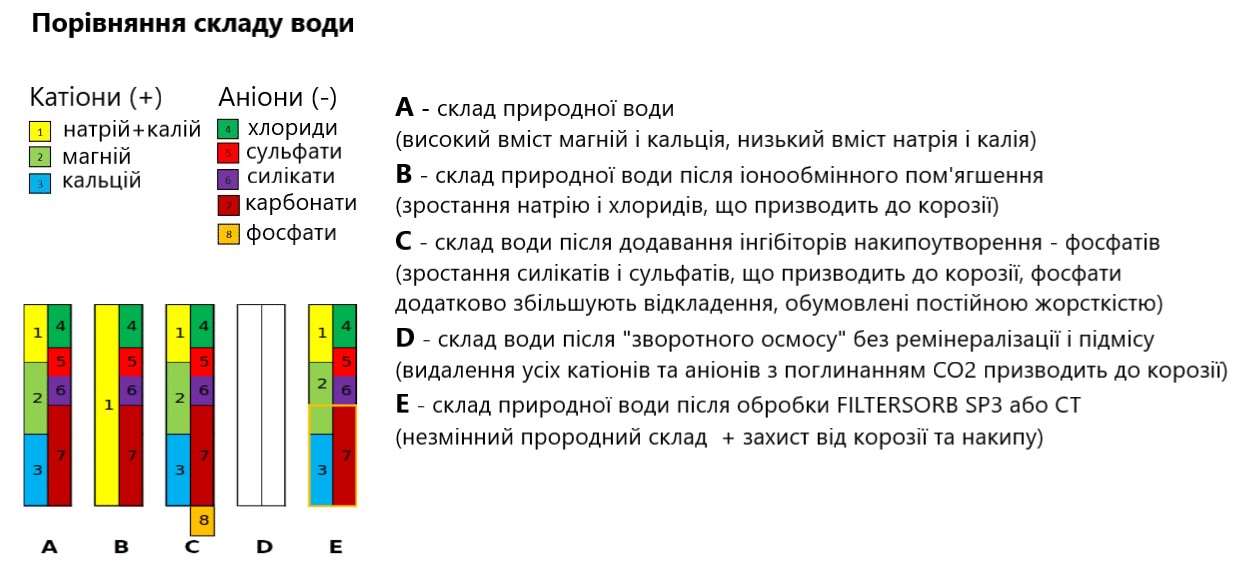
Технології, які на сьогоднішній день застосовують у водопідготовці для контролю накипоутворення в комунальному та побутовому секторі:
- Фосфати (поліфосфати). Секвестування солей карбонатної твердості.
Фосфати вперше були застосовані у водопідготовці далекого 1887 року. У 30-х роках XX століття дозування фосфатів у воду набуло широкого застосування дозування у воду 2 мг/л порошку гексаметафосфату натрію для контролю карбонатних відкладень у трубопроводах. У 70-х роках поширення набула технологія дозування фосфату цинку у воду з низькою жорсткістю для зниження її корозійної активності.
Фосфати втрачають ефективність при загальній жорсткості більше 3 мг-екв/л. Дозування фосфатів призводить до зростання загальної мінералізації та рН, що сприяє розмноженню бактерій у водопровідній системі. Дозування повинно здійснюватись автоматично або вручну контрольовано зі збереженням пропорції 2 мг/л. Вода із загальною жорсткістю більше 3 мг-екв/л вимагала застосування інших технологій – іонного обміну чи зворотного осмосу.
Як наслідок, дозування фосфатів збільшує загальну мінералізацію, підвищує рН, знижує вміст CO2, не ефективне при загальній жорсткості більше 3 мг-екв/л, перешкоджає відкладенню карбонатного накипу, збільшує відкладення солей постійної жорсткості (фосфати збільшують постійну жорсткість). Технологія дозволяє усунути проблему відкладень карбонатної жорсткості, проте дозування фосфатів збільшує відкладення постійної жорсткості.
- Іонний обмін. Пом’якшення.
Іонний обмін для пом’якшення води вперше було застосовано 1903 року. Технологія дозволяє фізично «обмінювати» кальцій та магній, замінивши їх на еквівалентну кількість іонів натрію. Технологія змінює склад води: у воді замість гідрокарбонатів кальцію та магнію з’являється гідрокарбонат натрію (NaHCO3, питна сода),кожен 1 мг якого здатний звільнити 0,79 мг CO2. Вільна вуглекислота збільшує концентрацію іонів водню (Н+), знижує рН та знижує лужність. Не змінюючи еквівалентні концентрації іонів у воді, процес іонообмінного пом’якшення збільшує загальну мінералізацію води за рахунок різної еквівалентної ваги (кожні 20 мг кальцію або 12 мг магнію обмінюються на 23 мг натрію). Зміна сольового складу надає прямий вплив на смак води. Технологія вимагає застосування реагентів (таблетованої солі), громіздких корпусів та мікропроцесорного клапана управління, впливає на навколишнє середовище (при регенерації скидання в каналізацію хлоридів кальцію та магнію, що підвищують солоність природних джерел прісної води).
Внаслідок пом’якшення води «іонним обміном» знижується рН, збільшується кількість вільної вуглекислоти, знижується лужність, кардинально змінюється хімічний склад солей та збільшується загальна мінералізація. Технологія іонообмінного пом’якшення дозволяє усунути проблему відкладень карбонатної жорсткості, але підвищує корозійну активність води.
- Зворотний осмос. Демінералізація.
Процес не відрізняється швидкістю. Кожен літр демінералізованої води вимагає скидання в каналізацію щонайменше 2…3 літрів технологічної води з концентрованими домішками. Всі трубопроводи і запірна арматура повинні бути виконані з пластику, тому що повністю демінералізована вода має кислу реакцію (контакт з атмосферним CO2) та, відповідно, високою корозійною активністю. Для нормального використання такої води потрібна повторна мінералізація. Загальна жорсткість понад 2,5 мг-екв/л суттєво скорочує термін служби мембрани.
- Каталітична кристалізація солей жорскості (NAC-технологія).
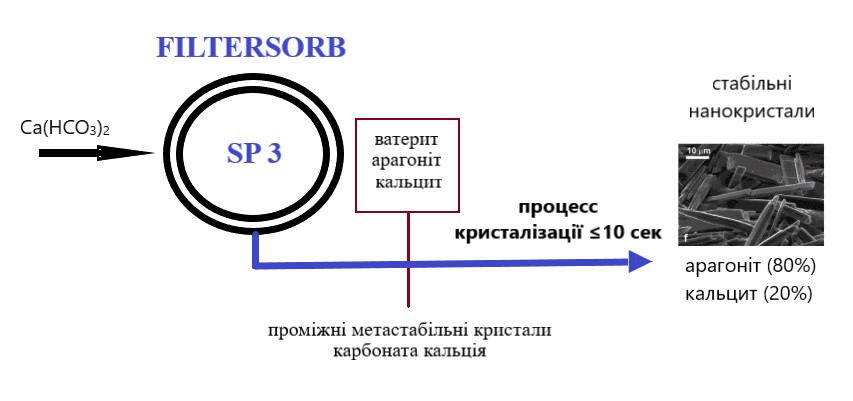
FILTERSORB SP-3 (Scale Prevention 3) вказує на результат трансформації розчинених гідрокарбонатів кальцію в три компоненти: CaCO₃ (мікрокристали арагоніта), CO₂ (вільна вуглекислота в колоїдній формі) та H₂O (чиста вода).
Этап 1. Керамічні кульки зі спеціальним покриттям FILTERSORB SP3 активують і контролюють процес трансформації гідрокарбонатів кальцію і магнію в нерозчинні наночастинки кристалів арагоніту, які не «прилипають» до поверхонь і перебувають у колоїдному стані. На сьогоднішній день FILTERSORB SP3 єдине доступне середовище, що викликає трансформацію такого роду.
Этап 2. У процесі руху через трубопроводи та побутові прилади вода, оброблена FILTERSORB SP3, видаляє раніше відкладений карбонатний накип.
Этап 3. Після видалення накипних відкладень FILTERSORB SP3 формує на трубах, кільцевих ущільненнях та проточних компонентах обладнання гладкий захисний шар арагоніту товщиною від 3 до 5 мкм, що перешкоджає корозії.
Загальна мінералізація та рН води залишаються незмінними. Домішки не видаляються. Корозійна активність води не збільшується.
*Водневий показник рН – міра кислотності та лужності розчину.
**Загальна жорсткість характеризує кількість розчинених у воді солей лужноземельних металів.
***Лужність характеризує здатність води чинити опір зміні рН.
****Вуглекислий газ знаходиться у воді у зв’язаній (карбонат-аніони CO32-), напівзв’язаній(гідрокарбонат-аніони HCO3–) та вільній (газоподібний CO2 та вугільна кислота H2CO3) формах. Вуглекислий газ безпосередньо впливає на рН, представляючи основне джерело кислотності у воді. Чим більше вуглекислоти, тим нижче рН.

