| ◄ 9 | 10 | 11 ► |
Розташування та установка модуля УФ-стерилізації VIQUA.
![]()
Рекомендації VIQUA щодо побудови ідеальної побутової схеми стерилізації води ультрафіолетом зі стадіями попередньої підготовки, байпасами, допоміжним обладнанням – клапаном регулювання температури та електромагнітним клапаном перекривання потоку на випадок аварійного відключення електроенергії. Схема містить опціональні компоненти, не обов’язкові для застосування в побутовому варіанті водопідготовки. Обов’язковою вважається умова наявності у схемі фільтра з рейтингом механічної фільтрації 5 мкм. Інші додаткові стадії попередньої підготовки визначаються якістю вихідної води.Читати повністю →
Katalox Light. Перше промивання.
![]()
Katalox Light – це високотехнологічне, повністю вироблене в Німеччині гранульоване фільтруюче середовище, що застосовується в задачах видалення заліза, сірководню, марганцю, миш’яку та радіонуклідів у системах побутової та комерційної водопідготовки. Унікальний склад і можливість працювати практично з будь-яким окислювачем надає Katalox Light очевидні переваги в порівнянні з такими популярними середовищами як Birm, Greensand Plus або Pyrolox, що мають низку серйозних обмежень. Після заповнення корпусу фільтра гравієм та середовищем Katalox Light виробник рекомендує виконати просту процедуру початкового промивання завантаження від пилоподібних частинок та шару дрібних фракцій “нижнього просіву”. Читати повністю →
Ультрафіолет не “вбиває” бактерії, паразити та вируси, але змінює структуру ДНК та запобігає їх розмноженню.
![]()
Позбавити свою систему водопостачання від мікробіологічного забруднення можна різними методами, наприклад, додаючи у воду хімічні речовини, фільтруючи воду через «щільний» керамічний фільтр або «відключаючи» репродуктивну функцію мікроорганізмів ультрафіолетовим випромінюванням. І якщо у випадку з хлоруванням або озонуванням Ви вестимете з мікроорганізмами у воді повномасштабну «хімічну війну» з різним успіхом і наслідками для кожної із сторін конфлікту, то у випадку з бактерицидним ультрафіолетовим випромінюванням Ви задіяєте «програму» стерилізації та контролю відтворення без будь-яких побічних ефектів. Читати повністю →
“Лернейска гідра” корозії або чому руйнуються металеві труопроводи.

Переважна більшість муніципальних водопроводів в Україні виготовлена з металу. Багато внутрішніх систем водопостачання котеджів містять мідні або сталеві трубопроводи та арматуру з латуні. Корозія металевих водопровідних труб пояснюється багатьма причинами і не всі причини корозії досі вивчені та зрозумілі. Результат корозії – руйнування поверхні трубопроводу та погіршення якості води. Деякі причини корозії прості і їх легко усунуті, інші – складні та важко діагностуються. Найчастіше корозія трубопроводу носить характер, що пояснюється сукупністю причин. Читати повністю →
Напірна аерація води. Відповіді на запитання.
![]()
Компресор нагнітає атмосферне повітря і створює “повітряну кишеню”, що займає приблизно 1/3 частину у верхній частині контактної ємності. Вода з такими «популярними» домішками як залізо, марганець і сірководень, надходить у фільтр через аераційну ємність з повітряною кишенею, наповненою стисненим атмосферним повітрям. Домішки окислюються в контактній ємності, фільтр затримує окислені домішки, кисень витрачається на окислення домішок та відновлення каталітичних центрів фільтруючого середовища. Напірна система аерації – це не фільтр, а стадія попередньої підготовки домішок для подальшої простої фільтрації у шарі завантаження фільтра-знезалізника, що йде за контактною аераційною ємністю. Читати повністю →
Katalox Light та H2O2.
![]()
В умовах позитивного значення ОВП оброблюваної води допускається застосування фільтруючого середовища Katalox Light без окислювача. Однак більшість завдань видалення заліза і сірководню в побутовій водопідготовці передбачають наявність у воді достатньої кількості окислювача. Подача окислювача (атмосферного кисню, перекису водню або хлору) може вимагати застосування дозуючих насосів або аераційного обладнання. Для окислення найважчих домішок у масивних концентраціях компанія-виробник Katalox Light рекомендує застосовувати перекис водню H2O2, функцію активації якого виконує каталітичне середовище Katalox Light. Katalox Light має здатність перетворювати H2O2 на гідроксид-радикали, окислювальна дія яких поступається тільки фтору. Читати повністю →
Кремній у воді. Доступні технології видалення.
Проблема необхідності видалення розчиненого кремнію завжди вносила сум’яття в уми продавців систем водопідготовки. Діоксид кремнію (SiO2) міститься в різних концентраціях у всіх природних водах. Хімія кремнію за складністю поступається лише хімії вуглецю. Тверде з’єднання діоксиду кремнію – кварц. Кварц інертний, але при поєднанні певних умов (дуже висока температура та лужне середовище) слабо реагує з водою, утворюючи кремнієву кислоту. У водопідготовці кремній та його сполуки розглядаються як забруднюючі речовини. Читати повністю →
Активні форми кисню. Пероксид водню та гідроксильний радикал.
![]()
Звичайні молекули містять на зовнішній орбіталі електронної оболонки два спарені електрони. Взаємодія магнітних моментів цих електронів забезпечує молекулі хімічну стабільність. Радикал характеризує наявність на зовнішній орбіталі одиночного (неспареного) електрона, що зумовлює виняткову хімічну активність частки, що прагне повернути ще один електрон у зовнішню орбіталь у процесі взаємодії з іншими частинками. Фактично молекула триплетного кисню О2, володіючи двома неспареними електронами, також є радикал (бі-радикал), що пояснює підвищену хімічну активність молекулярного кисню. Читати повністю →
H2O2 у водопідготовці. Видалення сірководню та заліза.
![]()
Запах сірководню – одна з найпоширеніших проблем води із свердловин. Історично в побутовій водопідготовці склалося так, що фізична аерація або хімічне хлорування стали звичайними способами усунення запахів води, викликаних вмістом леткої органіки, сірководню та інших розчинених газів. Однак, хлорування води пов’язане зі створенням небажаних «побічних продуктів» і вимагає введення досить високих доз для усунення сірководню при рН >7,5, а атмосферний кисень не має дезінфікуючої дії, не здатний зруйнувати залізо, вбудоване в органічні ланцюжки, не здатний усунути проблему залізобактерій. Перекис водню H2O2 діє ефективніше за атмосферний кисень, швидше за хлор, не створює побічні продукти, не вносить у воду сторонній смак і запах, не залишає “слідів”. Читати повністю →
Системи знезалізнення води на основе дозування хлора.

Хлор – відносно слабкий окислювач та сильний дезінфектор. Тому використання систем дозування рідкого хлорвмісного реагенту в задачах видалення заліза і дезінфекції води передбачає наявність у схемі нижче потоку від точки введення реагенту контактної ємності із забезпеченням експозиції близько 20 хвилин. Наприклад, якщо пікова швидкість очищення води від заліза становить 30 літрів за хвилину, для дотримання “правила експозиції” повинна застосовуватися контактна ємність об’ємом 600 (!) літрів. Розмір вражає для побутової водопідготовки? Однак, не все так погано як здається на перший погляд. Читати повністю →
Концентрація реагента Н2О2. Об’єм дозування. Налаштування дозувального насоса.
![]()
Дозування H2O2 на одиницю об’єму води безпосередньо залежить від концентрації окислюваних домішок. Одиниці виміру окислюваних домішок – міліграми на літр. Доза перекису водню H2O2 подається у воду пропорційно обсягу і витрачається на окислення різних домішок, що вступають у взаємодію з перекисом. Після реакцій окислення заліза, марганцю, сірководню, летких органічних речовин, що передбачають певний час контакту, оброблена вода, перед надходженням у фільтр з активованим вугіллям, повинна містити деяку залишкову кількість незв’язаного перекису водню ( 0,2…0,6 мг/л). Читати повністю →
Хімія “іонного обміну” або скільки натрія додає у воду пом’ягшувач.
![]()
Іонний обмін – на сьогоднішній день одна з найкращих технологій селективного видалення з води небажаних домішок. Класичний пом’якшувач води, дія якого заснована на технології “іонного обміну”, функціонує на принципах селективності та тяжіння позитивно заряджених іонів. Процес пом’якшення води збільшує показник загальної мінералізації води, але не змінює еквівалентні концентрації іонів у воді. Читати повністю →
Видалення амонія “іонним обміном”. Селективність або що може піти не так.
![]()
Для видалення з води амонію (NH4+) застосовують іонообмінні “пом’якшувачі”, що регенеруються розчином хлориду натрію (NaCl). Селективність стандартних катіонітів по амонію (коефіцієнт селективності 1,29) вище за селективність по натрію (коефіцієнт селективності 1). Бльша селективність амонію дозволяє витісняти зі смоли натрій. Але, що відбувається коли ємність смоли наближається до виснаження або вміст у воді солей жорсткості набагато перевищує вміст амонію (коефіцієнт селективності кальцію – 2,61 і магнію – 1,66)? Що може піти не так з видаленням “іонним обміном” амонію? Читати повністю →
Форми заліза та “іонний обмін”.

Виробники іонообмінних смол не здатні чітко пояснити, скільки заліза може бути видалено одночасно з пом’якшенням води. У цій статті ми спробуємо розібратися, як поводиться стандартна катіонообмінна смола з різними формами заліза в оброблюваній воді. Якщо вода містить залізо більше 5 мг/л, а форми присутності заліза у воді різні є висока вірогідність створення умов для незворотного отруєння смоли. Іонообмінна смола зберігає ефективність тільки щодо двовалентного розчиненого заліза. У завданнях видалення заліза «іонним обміном» особливу важливість набуває частота регенерацій, низький рН води і відсутність контакту води з киснем. Читати повністю →
Видалення з води нітратів. Технологія “іонного обміну”.
![]()
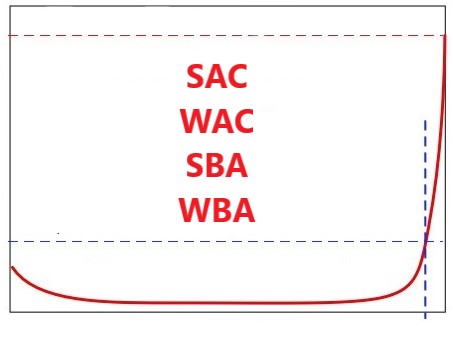
Нітрати з води селективно видаляють на основі застосування технології «іонного обміну» з використанням сильноосновної аніонообмінної смоли у хлоридній формі (SBA(Cl)), що регенерується розчином натрію хлориду (NaCl). Застосовують один із двох типів сильноосновних аніонообмінних смол – стандартну смолу та нітрат-селективну смолу. Іонний обмін нітратів на хлориди також супроводжується неселективним обміном сульфатів та на початку робочого циклу смоли також гідрокарбонатів. Пріоритетність сорбції для кожного аніону визначається шкалою селективності аніонообмінної смоли. Читати повністю →
Робоча обмінна ємність. Практичене значення.
Робоча обмінна ємність – це частина загальної обмінної ємності смоли (загальна кількість “активних груп”), що вимірюється в грам-еквівалентах на літр і вказує на кількість іонів (зарядів), здатних до обміну протягом робочого циклу до початку наступної регенерації. Таблиця з типовими значеннями загальної обмінної ємності для різних типів іонообмінних смол та приклади теоретичного та експериментального визначення робочої ємності сильнокислотного катіоніту – смоли, що застосовується для пом’якшення води. Читати повністю →
Іонний обмін. Межа солоності води.
![]()
Технологія іонного обміну – ідеальний інструмент для видалення або обміну домішок, які є у воді в низьких концентраціях. Однак, коли концентрація домішки в розчині висока (наприклад, кілька грамів на літр води) цикли іонного обміну стають надзвичайно короткими, а кількість реагенту для регенерації та технологічної води для промивання збільшується до вкрай неекономічного рівня – об’єм води для регенерації перевищує об’єм очищеної води. Якщо вихідна вода має високу солоність (досягнуто межу солоності) іонний обмін стане неприйнятною технологією обробки води і перевага повинна віддаватися «зворотному осмосу» або дистиляції. Читати повністю →
Базові процеси “іонного обміна” у водопідготовці. Як змінюється склад води.
![]()
Природна вода містить кальцій і магній, що формують солі з “дуже нестійкою” розчинністю. Катіони кальцію та магнію, спільно з менш поширеними іонами стронцію та барію, називають “іонами жорсткості”. Будь-яке випаровування (зміна об’єму) води призводять до втрати розчинності частини цих солей і утворення твердого осаду на поверхнях. Нагрів води призводить до утворення накипних відкладень. І навіть прості зміни швидкості руху/тиску води (наприклад, вилив холодної води через форсунки в системах зрошення) призводить до втрати розчинності солей жорсткості. Тут ми розповімо про пом’якшення, зниження лужності та вмісту нітратів, інші іонообмінні процеси, реакції іонного обміну та зміни, що вносяться “іонним обміном” до складу обробленої води. Читати повністю →

