Главная > Статьи > Страница8
Знезалізнення та видалення сірководню з води. Дозування перекису водню.
Технологія.
Перекис водню – один із найсильніших окислювачів. Окислення заліза та сульфіду потребує меншої концентрації перекису водню порівняно з хлором. Окислювальний потенціал перекису водню в 28 разів вище, ніж у хлору. Перекис водню на відміну хлор-реагентів містить лише атоми водню і кисню та не створює побічні продукти. Перекис розщеплюється у питній воді з виділенням активного атома кисню. Попередня стадія окислення перекисом водню складається із звичайного перистальтичного або мембранного насоса, резервуара для зберігання водного розчину пероксиду, статичного міксера для інтенсифікації масообміну та фільтра-знезалізнювача з протиточним способом промивання для видалення окисленого заліза. Для окислення заліза застосовують стандартний 7% водний розчин перекису водню, безпечний у побутовому варіанті використання.
Фільтрація.
Після обробки води перекисом водню для видалення окисленого заліза та сірки застосовують фільтр з гранульованим завантаженням та протиточною регенерацією. При виборі середовища віддають перевагу гранульованому активованому вугіллю, в ідеалі – активованому вугіллю з посиленими каталітичними властивостями (Chemviron Carbon Centaur, Sorboscarbon GAC PLUS, Jacobi Aquasorb CX-MCA). Популярні фільтруючі завантаження Birm і Pyrolox з перекисом водню НЕ ВИКОРИСТОВУЮТЬСЯ – перекис водню руйнує ці завантаження. Стандартне і каталітичне вугілля разом з окисленим залізом і сірководнем (сульфідом) розщеплюють і видаляють залишковий перекис.
Стабільність розчину та зберігання.
Перекис водню не відрізняється стабільністю. При застосовуваній у водопідготовці стандартної концентрації в 7% у баку для зберігання розчину перекис водню розкладається до Н2О і втрачає на місяць близько 2% концентрації. Швидкість розкладання перекису водню ще вища зі зростанням концентрації — 50% розчин знижує протягом місяця концентрацію до 25% (!). Стабілізований бензоатом натрію (0,05%) 6…7%-перекис водню зберігає свою концентрацію приблизно в 5 разів довше.
При застосуванні 35% розчину (концентрація — 350 гр/л, 350000 ppm) його розбавляють до 7% розчину (70 гр/л, 70000 ppm) водою (до 1 частини 35% розчину Н2О2 додають 4 частини дистильованої води). Розведення здійснюють максимально чистою водою, оскільки перекис водню реагує з домішками. Вода, очищена зворотним осмосом, також може застосовуватися для розведення.
Обмеження.
Максимальна концентрація заліза – 10 мг/л.
Максимальна концентрація сірководню не обмежена.
Дозування.
Видалення заліза з розрахунку 0,4 мг/л пероксиду водню на 1 мг/л заліза у воді.
Видалення сірководню з розрахунку 1 мг/л пероксиду водню на 1 мг/л сірководню у воді при рН = 7. Підвищення рН вимагатиме збільшення дози.
Час контакту.
Швидкість реакції окислення пероксидом заліза і сірководню набагато більша ніж у окислювачів, що містять хлор. Практично це означає, що у побутовому варіанті застосування замість контактної ємності достатньо статичного міксера, що прискорює масообмін.
Обладнання.
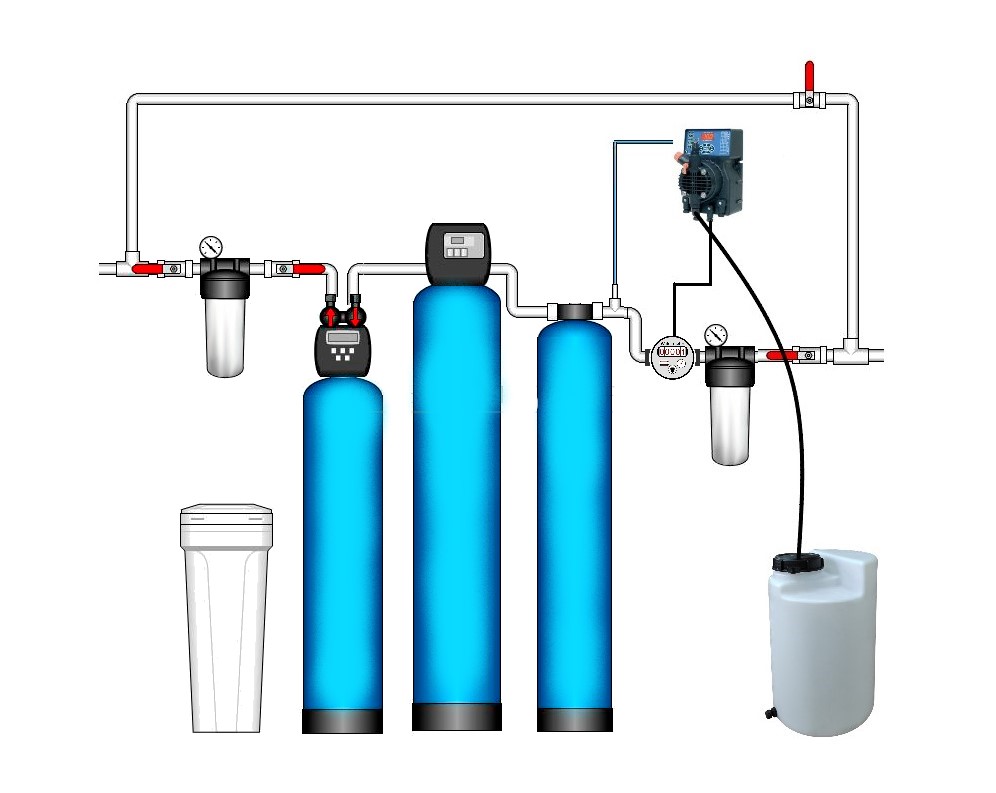
Для дозування пероксиду застосовують перистальтичний насос із низькою швидкістю подачі. Наявність контактної ємності необов’язкова. Замість контактної ємності застосовують статичний міксер, встановлений за напрямом потоку після точки дозування пероксиду. Дозування з фіксованою швидкістю у воду, що подається насосом із свердловини, здійснюється у трубопровід до гідроакумулятора. Фільтр із активованим вугіллям встановлюють після гідроакумулятора. Іонообмінний пом’якшувач встановлюють після фільтру з активованим вугіллям.
Приклад розрахунку дозування в воду розчину Н2О2 7%.
Об’ємна швидкість потоку води — 37,5 л/хв ( 10 GPM).
Концентрація заліза у воді — 5 мг/л.
Вихідна концентрація в розчині 7% Н2О2 — 70000 ppm ( 70 гр/л, 70000 мг/л).
Необхідна концентрація Н2О2 = 5 мг/л Fe x 0,4 мг/л = 2 ppm (2мг/л).
1440 — кількість хвилин на добу.
Об’єм дозованого розчину 7% Н2О2 = 37,5 л/хв (10 GPM) x 2 ppm (5мг/л Fe) x 1440 / 70000=0,41 GPM = 1,55 літра на добу розчина 7% Н2О2 або 0,065 літров на годину розчина 7% Н2О2.

