![]() До появления современных ионообменных процессов единственным способом получения чистой воды была дистилляция. Вопреки распространённому мнению одноступенчатая дистилляция не позволяет получить химически чистую воду. Фактически, для достижения чистоты воды, полученной при ионном обмене в процессе деионизации, потребовалось бы более 20 последовательных дистилляций с использованием инертных кварцевых сосудов.
До появления современных ионообменных процессов единственным способом получения чистой воды была дистилляция. Вопреки распространённому мнению одноступенчатая дистилляция не позволяет получить химически чистую воду. Фактически, для достижения чистоты воды, полученной при ионном обмене в процессе деионизации, потребовалось бы более 20 последовательных дистилляций с использованием инертных кварцевых сосудов.
Общие положения.
- Удаление всех примесей из воды и получение высококачественной воды называется процессом деионизации (DI).
- Деионизированную воду можно получить разными методами, но в этой статье мы рассматриваем только метод ионного обмена.
- В процессе ионного обмена применяются катионообменные и анионообменные смолы, электростатически связанные с ионами водорода и гидроксильной группы соответственно.
- Смола смешанного действия сочетает катионообменную и анионообменную смолы в определённом соотношении.
- Смола смешанного действия более эффективна, чем двухслойные или двухстадийные системы деионизации.
- Смола смешанного действия со временем истощается, требует регенерации или замены.
- Ионообменная система («ионообменник») со смолой смешанного действия может использоваться для получения воды высокого качества из водопроводной воды (в т.ч. в резервных процессах), однако из-за высокой концентрации катионов и анионов в водопроводной воде фильтр смешанного действия быстро исчерпает свою емкость.
- Обычно система со смолой смешанного действия — последний этап в технологической цепочке получения сверхчистой воды. Система со смолой смешанного действия устанавливается после двухстадийного ионообменного деминерализатора или после системы обратного осмоса. При таком применение ионообмення система смешанного действия обеспечивает дополнительную очистку («полировку») ранее деминерализованной воды и способна продуцировать уже сверхчистую воду с удельным сопротивлением до 18,2 мОм х см (при этом сохраняя высокую производительность и срок службы в течение нескольких месяцев при правильном проектировании).
- При использовании «ионообменника» смешанного действия с системой обратного осмоса производительность может существенно снижаться из-за поглощенного пермеатом атмосферного CO2. Этот CO2 не отображается контроллером электропроводности обратного осмоса, но будет удаляеться анионообменной смолой, сокращая общий срок службы смешанной смолы.
- Контроль исчерпания рабочей емкости «ионообменника» смешанного действия может осуществляться простым встроенным измерителем сопротивления.
- При исчерпании емкости замена смолы смешанного действия – наиболее логичное и простое решение, не требующее организации сложного процесса регенерации.
- Фильтры смешанного действия — отличный способ удалить остаточное солесодержание и реактивный кремний из воды после установки обратного осмоса (в отличии от коллоидного кремния реактивный кремний не удаляется механической фильтрацией).
- В рабочем цикле вода поступает в корпус со смешанной смолой через верхний дистрибьютор в направлении сверху-вниз.
- Смола смешанного действия позволяет получить сверхчистую воду, однако процесс регенерации может оказаться слишком сложным. До начала регенерации смолы необходимо гидравлически разделить на два отдельных слоя (катионит и анионит) противоточной промывкой за счет разной плотности. Регенерация требует большого количества реагентов (кислота и щелочь) и сложной организации циклов. Поэтому смолы смешанного действия обычно применяются для «полировки» предварительно деминерализованной воды до уровня электропроводности воды 1 мкСм/см и ниже и заменяются без регенерации.

Ионный обмен. Процессы.
Создание полимера с названием «стирол-дивинилбензол» проложило путь к созданию современных сильноосновных анионообменных (SBA) и сильнокислотных катионообменных смол (SAC), применяемых в ионообменных процессах.
Процесс ионного обмена легко визуализировать. Слой из нерастворимых полимерных шариков смолы, содержащих активные центры (функциональные группы) с обмениваемыми ионами, помещается в корпус, через который протекает поток воды. Ионы из воды избирательно притягиваются к активным центрам смолы, обмениваясь с ионами, связаными с активным центром. Этот процесс создает новый состав воды, с другими химическими свойствами.
Пример такого изменения состава – процесс умягчения с применением сильнокислотного катионита в натриевой форме (с обменным натрием в активном центре).
 В ходе процесса умягчения катионы кальция и магния заменяются на катионы натрия, который устраняет проблему накипеобразования и рассматривается как более приемлемый ион для многих применений воды. Однако, если умягченная вода будет использована для питания парового котла, гидрокарбонаты натрия в составе умягченной воды при перегреве и образровании пара будут разрушаться с выделением агрессивного углекислого газа. Для устранения этой проблемы из питающей воды нужно удалить щелочность и создать другой состав воды в процессе ионного обмена — заменить анионы гидрокарбоната на анионы хлорида. Хлориды не испаряются и не выделяют углекислый газ.
В ходе процесса умягчения катионы кальция и магния заменяются на катионы натрия, который устраняет проблему накипеобразования и рассматривается как более приемлемый ион для многих применений воды. Однако, если умягченная вода будет использована для питания парового котла, гидрокарбонаты натрия в составе умягченной воды при перегреве и образровании пара будут разрушаться с выделением агрессивного углекислого газа. Для устранения этой проблемы из питающей воды нужно удалить щелочность и создать другой состав воды в процессе ионного обмена — заменить анионы гидрокарбоната на анионы хлорида. Хлориды не испаряются и не выделяют углекислый газ.
 Ионообменный процесс снижения щелочности осуществляется с применением сильноосновного анионита II типа в хлоридной форме (с обменным хлоридом в активном центре).
Ионообменный процесс снижения щелочности осуществляется с применением сильноосновного анионита II типа в хлоридной форме (с обменным хлоридом в активном центре).
Ионообменная Деионизация (DI) — это двухэтапный процесс, при котором задействуется последовательно два слоя: первый слой катионита (с обменным водородом H+) и второй слой анионита (с обменной гидроксильной группой OH—) .
Первая реакция в слое катионита заменяет все катионы на ион водорода и превращает все анионы в кислоты.
 Вторая реакция в слое анионита замещает все анионы кислот, включая силикаты SiO2, на гидроксильную группу и нейтрализует воду. Конечный продукт – вода.
Вторая реакция в слое анионита замещает все анионы кислот, включая силикаты SiO2, на гидроксильную группу и нейтрализует воду. Конечный продукт – вода.
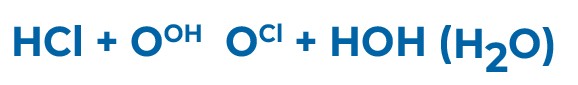 Логично предположить, что процесс деионизации из двух слоев можно было бы заменить их точной смесью в так называемом смешанном слое (английское название — mixed bed). В 1949 году впервые использовали смешанные слои и получили воду высокого качества. Единственным, но крайне неудобным недостатком стало то, что для регенерации смол их приходилось тщательно разделять. Поэтому двухслойная концепция последовательной деионизации в двух отдельных корпусах осталась более практичной, удобной и менее затратной – для регенерации смолы не нужно было извлекать из корпусов и разделять. Применение трехслойной деионизации (катионит-анионит-катионит) позволяло без смешивания слоев получить еще более чистую воду с удельным електрическим сопротивлением около 1 мОм х см.
Логично предположить, что процесс деионизации из двух слоев можно было бы заменить их точной смесью в так называемом смешанном слое (английское название — mixed bed). В 1949 году впервые использовали смешанные слои и получили воду высокого качества. Единственным, но крайне неудобным недостатком стало то, что для регенерации смол их приходилось тщательно разделять. Поэтому двухслойная концепция последовательной деионизации в двух отдельных корпусах осталась более практичной, удобной и менее затратной – для регенерации смолы не нужно было извлекать из корпусов и разделять. Применение трехслойной деионизации (катионит-анионит-катионит) позволяло без смешивания слоев получить еще более чистую воду с удельным електрическим сопротивлением около 1 мОм х см.
Ионный обмен. Реакция равновесия.
Ионный обмен – это реакция равновесия. Если конечный продукт декатионирования вода с кислотой и кислота используется для регенерации, то катионит будет испытывать некоторое увеличение нагрузки по мере увеличения общего солесодержания (TDS) в исходной воде. Чем выше TDS, тем больше кислоты в конечном продукте (в обработанной в слое катионита воде) и тем ниже pH. В определенный момент pH воды может стать достаточно низким, чтобы начать регенерацию катионита, что приведет к вытеснению ранее обменяных катионов, преимущественно натрия. Вытесненный натрий превратится в следующем слое анионообменной смолы в гидроксид натрия, что приведет к росту рН (больше 10) и ограничит применение этой воды. Если мы посмотрим на равновесное соотношение натрия/водорода для катионного обмена, то легко увидим, что происходит:
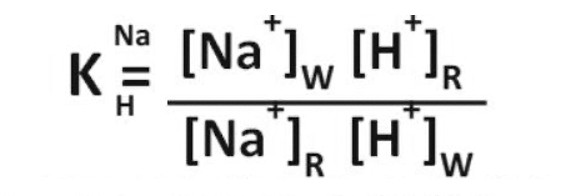 Это уравнение показывает, что соотношение для катионообменной смолы в форме H+ будет зависеть от концентрации натрия в воде [Na+]W и концентрации водорода на смоле [H+]R. Таким образом, чем выше солесодержание воды и чем лучше регенерация, тем больше это равновесие смещается вправо. По мере истощения емкости слоя и, соответственно, одновременного повышения концентрации натрия на смоле и концентрации водорода в воде, значения в нижней части уравнения увеличиваются, и равновесие смещается влево — наступает предел, после которого утечка натрия увеличивается.
Это уравнение показывает, что соотношение для катионообменной смолы в форме H+ будет зависеть от концентрации натрия в воде [Na+]W и концентрации водорода на смоле [H+]R. Таким образом, чем выше солесодержание воды и чем лучше регенерация, тем больше это равновесие смещается вправо. По мере истощения емкости слоя и, соответственно, одновременного повышения концентрации натрия на смоле и концентрации водорода в воде, значения в нижней части уравнения увеличиваются, и равновесие смещается влево — наступает предел, после которого утечка натрия увеличивается.
Вода высокой степени чистоты без смешанных слоев.
По мере того, как pH очищенной воды (как из катионообменного, так и из анионообменного слоя) отклоняется от значения 7, равновесная реакция замедляется и препятствует протеканию ионообменных реакции. Следовательно, по мере увеличения общего солесодержания (TDS) увеличивается утечка натрия. По мере увеличения утечки натрия увеличивается и pH анионного продукта, что, в свою очередь, увеличивает утечку SiO2. При отклонении pH обоих продуктов от значения 7 двухступенчатая система DI будет ограничена по общему солесодержанию (TDS). Опыт подсказывает, что этот предел TDS составит около 2000 мг/л. Однако, установка двух или более двухступенчатых систем подряд решит эту проблему. В целом, катионообменный слой системы DI снижает содержание катионов в воде на 99,5%. Это означает, что при подаче воды с солесодержанием 1000 мг/л будет наблюдаться утечка натрия около 5 ppm. При движении через анионит натрий преобразуется в гидроксид натрия и результирующий pH составит около 10, а удельное сопротивление обработання воды — около 60 кОм.
Этого может оказаться достаточным для автомойки, но не более того. Однако, если эту же очищенную воду подать на другой катионит, снижение pH до 7 будет весьма благоприятным. Если мы увидим дополнительное снижение содержания катионов на 99%, то на выходе из «повторного» слоя катионита концентрация натрия составит менее 0,1 мг/л. Одного этого достаточно, чтобы увеличить удельное сопротивление воды почти до 1 мОм х см. Добавьте ещё один анионит, и сопротивление более 1 мОм х см можно будет достичь даже без использования смешанного слоя со сложным процессом регенерации.
Система деионизации со смолой смешанного типа.
Идея нескольких последовательных циклов деионизации привела к разработке системы смешанного типа. Если два цикла катионирования способны поднять удельное сопротивление с 60кОм х см до 1 мОм х см, то на что потенциально способны несколько десятков циклов катионирования/анионирования? Ответ — мы можем получить очищенную воду с удельным сопротивлением более 18,2 мОм х см. Измерить удельное сопротивление воды, превышающее это значение, практически невозможно, поскольку сверхчистая вода становится автоионной, начинает ионизироваться, превращаясь в проводимое вещество. В литературе указано, что максимальное удельное сопротивление для сверхчистой воды составляет 18,2 мОм х см. Соответствующее этому удельному сопротивлению значение TDS составляет менее 0,03 ppm. Даже плохо регенерированный смешанный слой может производить воду с удельным сопротивлением около 10 мОм х см.
Соотношение катионита и анионита.
Реакция ионного обмена протекает в разбавленных растворах. По мере прохождения исходной воды через смешанный слой (mixed bad) и замещения заряженых ионов водой, общее солесодержание (TDS) снижается, и реакция успешно завершается. Таким образом, рабочая ёмкость смешанной смолы может быть очень близка к общей ёмкости соответствующих смол катионита и анионита в двухслойной системе. В двухслойной системе соотношение емкости SAC и SBA составляет примерно 2:1. Однако в смешанном слое соотношение ближе к абсолютной общей ёмкости 1,95:1,2. Поскольку ёмкость у катионита на 50% выше, чем у анионита, мы компенсируем это соотношение, создавая смешанный слой с 60% анионита и 40% катионита. Эта пропорция обеспечивает небольшое преимущество в ёмкости по катионам и препятствует загрязнению анионита солями жёсткости. Преимущество смешанного слоя заключается не только в получение воды более высокой степени чистоты, но и в большей производительностии в сравнении с двухстадийной системой DI. В смешанном слое обрабатываемая вода многократно «полируется» посредством непрерывных и одновременных реакций ионного обмена катионов и анионов, что приводит к получению воды с очень низкой электропроводностью до 0,05 мкСм/см (высоким удельным сопротивлением до 18,2 мОм х см).
Системы деионизации со смешанным слом традиционно применяются как последующая стадия «полировки» частично деминерализованной воды в результате другого процесса деминерализации — обратного осмоса, двухстадийной ионообменной деминерализации или дистиллирования. Потребность в сверхчистой воде актуальна в энергетике, в производстве полупроводниковой электроники или фармацевтических препаратов. Двойная природа смолы смешанного действия позволяет ей достигать уровней удаления ионов, значительно превосходящих возможности отдельных катионных и анионных слоёв.
Смола смешанного действия. Регенерация.
После исчерпания обменной емкости смола смешанного действия может быть регенерирована. До начала регенерации противоточной промывкой гидравлически разделяют смешанную смолу за счет разной плотности на два отдельных слоя — катионит и анионит. Раствор кауcтической соды (гидрооксида натрия NaOH) подают снизу в слой анионообменной смолы, раствор соляной кислоты (HCl) одновременно подают сверху в слой катионообменной смолы. Сброс отработанных растворов осуществляется одновременно через общий коллектор.
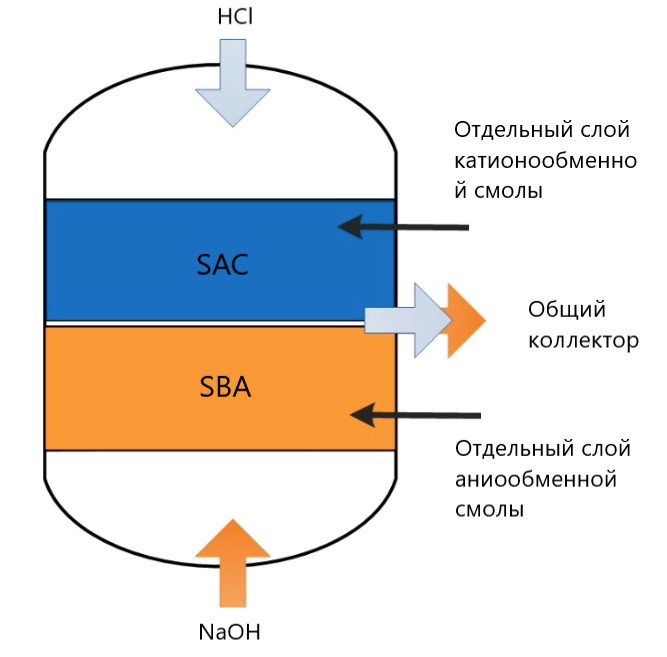
После регенерации слоев последовательно запускаются циклы: медленной промывки чистой водой для вытеснения остатков кислоты и щелочи, дренажа (удаление воды из слоев перед подачей воздуха), перемешивания сжатым воздухом, заполнения водой корпуса и прямоточной промывки.

