Определение жесткости.
Восприятие мягкой воды пользователями часто выходит за рамки простого предотвращения образования накипи. Вода, содержащая двухвалентные ионы кальция и магния, оставляет на контактных поверхностях твердый осадок при нагревании или испарении. Мы называем такую воду жесткой. Жесткость может быть «временной», связанной с анионами слабых кислот (преимущественно с анионами угольной кислоты – гидрокарбонатами, реже – силикатами или фосфатами) и постоянной, связанной с анионами сильных кислот (сульфатами, хлоридами, нитратами). Название временная жесткость получила так, как ее можно легко уменьшить простым нагреванием воды и преобразованием растворимой соли гидрокарбоната по реакции:
Ca(HCO3)2 = CaCO3 + CO2 + H2O
Эта формула объясняет причину, по которой в бойлерах и посудомоечных машинах образуется накипь и почему в промышленности для воды, питающей котельное оборудование, задействуют процессы снижения щелочности и умягчения, чтобы уменьшить как образование накипи, так и выделение кислотного коррозионно-агрессивного пара, содержащего CO2. Сам по себе традиционный процес умягчения не снижает коррозионную активность воды, так как приводит к выделению агрессивного CO2. Полученные в результате анионного обмена хлориды кальция и магния — не соли жесткости, накипь не создают, в осадок не выпадают ни при каких обстоятельствах.
Анионообменое «умягчение» (обезщелачивание воды).
Снижение щелочности позволяет устранить накипеобразование без выделения CO2. Если оператор сталкивается с питательной водой, щелочность которой превышает жесткость, а коррозионная активность является большой проблемой для водонагревательного оборудования, можно кондиционировать воду, используя анионообменную смолу (WBA или SBA), регенерируемую хлоридом натрия. Этот процесс приведет к замене всех анионов, включая гидрокарбонаты, на хлориды. В итоге, кипячение воды не приведет ни к образованию накипи, ни к выделению агрессивного CO2.
Формирование накипи.
Гидрокарбонаты кальция и магния растворимы, но не существуют в природе в виде сухих солей. При испарении воды даже при температуре окружающей среды, раствроенные гидрокарбонаты превращаются в нерастворимые карбонаты. Жесткая вода, оставленная высыхать, например, когда разбрызгиватели для газонов распыляют воду на металлический забор или автомобиль, образует твердую трудноудаляемую накипь. По этой причине на мойках либо используют обессоленую воду, либо вручную вытирают воду с металлических и стеклянных поверхностей, чтобы предотвратить появление пятен соли. Также вода, испаряющаяся с поверхности бассейна, образует твердую накипь на линии водораздела. Постоянная жесткость ведет себя иначе и не так склонна к образованию накипи при нагревании (тем не менее гипсовая накипь (сульфат кальция) может образовываться если вода содержит высокие концентрации сульфатов). Гипс также может выпадать в осадок при концентрировании раствора с высоким содержанием сульфата кальция, например, на поверхности мембраны обратного осмоса. Соль хлорида кальция (CaCl2) лучше растворяется в воде в сравнении с обычной солью хлорида натрия. CaCl2 не выпадает в осадок ни при каких условиях, но не остается долго в кристалличесткой форме (CaCl2 — гигроскопичная соль, впитывающая влагу из атмосферы). По этой причине эту соль часто применяют для посыпания грунтовых дорог, чтобы сохранять небольшую влажность поверхности и связывать пыль.
Если общая щелочность превышает общую жесткость, вся жесткость временная. Если жесткость превышает щелочность, присутствует как временная, так и постоянная жесткость. Как временная, так и постоянная жесткость реагируют с мылом, образовывая нерастворимый мыльный шлак, который мы видим в качестве кольцевого отложения на границе водораздела по периметру ванны. Мыло обычно представляет собой натриевую соль жирных кислот и растворяется в воде. Напротив, двухвалентные соли жесткости плохо растворимы. Мыло действует как «ионообменник», реагирует с двухвалентными ионами жесткости и осаждает их. Всякий раз, когда жесткая вода и мыло смешиваются, сначала необходимо добавить достаточное количество мыла, чтобы осадить всю жесткость, а затем достаточное количество мыла для выполнения моющего действия. В душе мыло и шампунь, кажется, легче смываются жесткой водой. Но смываются ли они на самом деле? Нет! Они осаждаются на коже в виде щелочного остатка и становятся причиной раздражения кожи, сухости и ломкости волос.
Кроме того, многие чистящие средства используют щелочные усилители для повышения pH, поскольку масла и грязь легче смываются водой с более высоким pH. Однако более высокий pH также преобразует соли гидрокарбоната в соли карбоната, которая затем выпадает в осадок. При еще более высоком pH все формы жесткости теряют растворимость и осаждаются, создавая ефект мутной воды. Это причина, по которой жесткая вода не может применяться для регенерации анионообменной смолы в системах деионизации, регенерируемых гидроксидом натрия. Бытовые и промышленные пользователи жесткой воды сталкиваются с дополнительными расходами на замену оборудования из-за накипи или дополнительными трудозатратами на устранение отложений, ограничением потока из-за накипи в трубах и дополнительными энергетическими затратами на нагрев воды.
Можно обобщить преимущества использования мягкой воды, просто перечислив недостатки использования жесткой воды:
— жесткая вода образует осадок в виде карбонатной накипи при нагревании.
— жесткость образует осадок при повышенном pH.
— жесткость образует осадок при увеличении концентрации (например, снижение объема воды вследствии испарения).
— твердая накипь образуется при простом испарении жесткой воды.
— жесткая вода реагирует с мылом, образуя нерастворимый мыльный шлам.
Определение мягкой воды.
Умягченная вода не делает ничего из перечисленного выше. По определению WQA мягкая вода — это вода, которая содержит жесткость менее 0,34 мг-екв/л (<17,1 мг/л по CaCO3). Любое устройство для кондиционирования воды, которое снижает жесткость исходной воды до уровня менее 0,34 мг-екв/л, является, таким образом, умягчителем. Любое устройство для кондиционирования воды, которое не снижает жесткость исходной воды до уровня ниже 0,34 мг-екв/л, соответственно, не может называться умягчителем, а вода, которую производит это устройство, не может называться мягкой. Устройство, которое снижает жесткость исходной воды, однако не до уровня ниже 0,34 мг-екв/л, также не может называться умягчителем. Не существует такого понятия, как частично умягченная вода, кроме воды, которую получают путем смешивания мягкой воды с жесткой.
Необходимы альтернативные технологии.
Большинство умягчителей воды основаны на технологии катионного обмена и используют соль хлорида натрия (NaCl) в качестве регенерирующего реагента. Современные умягчители обладают высокой эффективностью, т.е. используют лучшее соотношение расхода соли к объему обработанной воды. Также существуют умягчители, которые используют для регенерации хлорид калия (KCl) вместо хлорида натрия (NaCl). Такие умягчители иногда называют «безсолевыми» умягчителями, однако KCl — это тоже соль.
Действительно ли существуют устройства, которые можно было бы назвать бессолевыми умягчителями воды? Да, существуют. Мы знаем их как дистилляторы, системы обратного осмоса и нанофильтрации, деионизаторы (ионный обмен), системы емкостной деионизации (EDI). На сегодняшний день развитие альтернативных технологий умягчения без регенерации солью получило большой толчок. Основной движущей силой поиска альтернатив ионообменному умягчению стала необходимость в поддержании низкого уровня солесодержания (TDS) сточных вод, чтобы их можно было повторно обрабатывать для сброса в грунтовые воды без необходимости снижать TDS с помощью дорогостоящего оборудования. Необходимость в низком солесодержании сточных вод привела к появлению законов, ограничивающих использование ионообменных умягчителей воды, регенерируемых солью, в Калифорнии, Аризоне, Техасе, Коннектикуте, Мичигане и Неваде.
Предотвращение образования накипи.
Накипь представляет собой наибольшую проблему использования жесткой воды. На сегодняшний день существует несколько технологий, направленных на уменьшение образования накипи. Первая и наиболее распространенная технология — удаление ионов, образующих накипь, с помощью обычного ионообменного умягчителя, регенериремого солью. Бывают ситуации, когда из воды вместе с солями жесткости необходимо удалить почти все другие соли и тогда применяется технология деминерализации. Также существуют способы обработки воды химическими добавками либо предотвращающими образование накипи, либо делающими накипь более мягкой и легко удаляемой. Средства для предотвращения образования накипи работают на принципе изолирования солей жесткости с помощью химических добавок (хелатирующих веществ), которые эффективно связывают ионы металлов, делая их нереактивными. Пример такой добавки — ЭДТА (этилендиаминтетрауксусная кислота, «Трилон Б»). Другие добавки (например, низкие уровни полифосфата) вызывают образование мягкой накипи, вмешиваясь в кристаллическую решетку образования твердой накипи. Наконец, существуют устройства физической очистки воды, которые не удаляют ионы, образующие накипь, и не добавляют в воду химикаты:
— устройства, предотвращающие отложенние накипи (образующие микроскопические кристаллы твердой накипи в водной фазе, которые не позволяют накипи откладываться на поверхностях, блокировать поток и теплопередачу);
— устройства, предотвращающие образование твердой накипи, которые преобразуют кальцит в арагонит или какую-либо другую форму мягкой накипи, которая легче удаляется.
Все вышеупомянутые технологии продемонстрировали в разной степени способность уменьшать проблемы, связанные с накоплением твердой накипи. В нашем списке из пяти проблем с жесткой водой, упомянутых ранее, эти технологии решают проблему №1 — предотвращение образования накипи.
Варианты коммерческой и промышленной очистки воды.
Если основной проблемой является предотвращение образования накипи в котле с последующей потерей эффективности теплопередачи и затратами на техническое обслуживание, связанное с обширной очисткой, большинство из вышеперечисленных технологий найдут тот или иной уровень принятия у потребителя. Некоторые из них принимаются с большей готовностью, чем другие. Например, образование мягкой накипи некоторыми физическими технологиями водоподготовки все еще потребует периодических остановок оборудования для очистки. Технологии ионообменного умягчения и деминерализации фактически удаляют ионы жесткости и производят воду, которая не образует накипи.
Если Вы хотите получить все преимущества мягкой воды выбор технологий становится коротким. Реакционную способность двухвалентных катионов жесткости придется удалить из воды одним из методов удаления, перечисленных в таблице 1. Требуемый результат можно получить умягчением или деминерализацией либо используя для предотвращения реакций катионов такое химическое хелатирующее вещество, как ЭДТА. В таблице 1 показана эффективность различных технологий в отношении разных негативных проявлений жесткой воды.
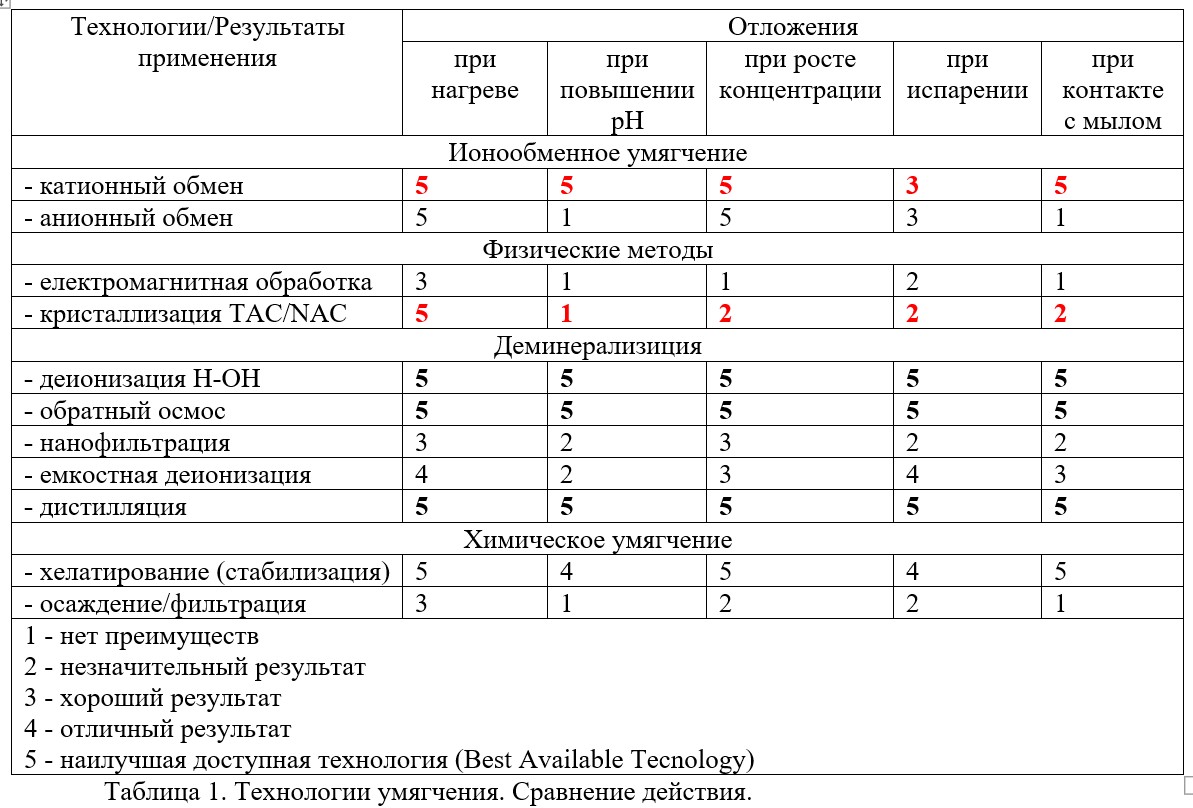
*катионное или анионное умягчение — отложения на поверхностях после испарения воды (пятна соли) не создают твердую или мягкуюмнакипь и не содержат соли жесткости.
Обсуждение таблицы 1.
Для проявления негативного действие в воде должны присутствовать ионы жесткости в достаточном количестве. Катионообменное умягчение, обратный осмос, деионизация и дистилляция — единственные процессы, которые удаляют двухвалентные ионы практически до нуля.
Анионный обмен удаляет противоионы (бикарбонаты и сульфаты). В итоге жесткость не создает накипь, но оставшиеся в растворе катионы кальция и магния будут реагировать с мылом и осаждаться при повышенном pH (в виде гидроксидов кальция и магния).
Обратный осмос (только при высоком давлении) обладает практически 100 % эффективностью в отторжении кальция и магния.
Нанофильтрация имеет более низкие показатели отторжения солей жесткости. Емкостные деионизаторы – относительно новые устройства, которые удаляют жесткость посредством электрического притяжения ионов к электродам с помощью постоянного тока и снижают образование накипи примерно до 95 процентов. Тем не менее, остаточная жесткость все еще позволяет воде реагировать с мылом и вызывать сильное помутнение воды при повышении pH. Химическое хелатирование по сути изолирует двухвалентные ионы так, чтобы они не могли вступать в реакции. Полученные хелаты не образуют накипь при нагревании или испарении, не реагирует с мылом. Химический хелатирующий реагент (например, ЭДТА) часто включается в чистящие составы специально для того, чтобы позволить мылу выполнять свою работу в жесткой воде.
В меньшей степени те химические добавки, которые позволяют накипи образовывать осадок, но препятствуют росту накипи, диспергируя микрочастицы, позволяют большому количеству реактивной жесткости оставаться в растворе. Сочетание осажденной накипи и новой твердой накипи оставляет осадок, который значительно мягче и легче удаляется. В растворе все еще содержится достаточно реактивной жесткости для реакции с мылом или помутнения воды при высоком pH. После применения технологии «холодного» известкования (снижение жесткости до 1…1.5мг-экв/л) обычно требуется ионообменная полировка для большинства применений. Технология «горячего» извескования позволяет снизить жесткость до значения менее 0,34 мг-экв/л. Технология известкования из-за химической сложности процесса и размера оборудования не подходит ни для чего кроме крупных промышленных или муниципальных применений.
Физические технологии умягчения воды делятся на две группы.
Первая группа:
— технологии, предотвращающие накипь, которая работает на принципе стимуляции образования накипи до поступления воды в водонагреватель. Эта группа включает технологию каталитической кристаллизации NAC (TAC), которая катализирует образование субмикронных кристаллов (кристаллы остаются в потоке воде в виде коллоидно-взвешенных частиц, которые не прилипают к нагретым поверхностям);
— технологии электрически индуцированого осаждения, которое образует мягкую накипь на электроде (необходима периодическая очистка).
Вторая группа:
— технологии предотвращения образования накипи, которая подразумевают изменение состава воды. К этой группе относится емкостная деионизация (которая фактически снижает солесодержание воды, притягивая растворимые ионы к селективным электродам) и электромагнитные устройства, которые, как утверждается, образуют мягкий осадок, состоящий из аморфных кристаллов арагонита и ватерита вместо более стойкой твердой формы накипи, называемой кальцитом.
На саммите Аризонского отделения WQA в ноябре 2010 года профессор инженерной экологии Университета Аризоны доктор Питер Фокс (Темпе, Аризона) представил доклад(1) с промежуточными результатами исследований альтернативным устройствам для очистки воды. В частности, его исследования представляют собой оценку альтернатив регенерируемым бытовым умягчителям воды. Выбранные для исследования устройства были основаны на различных технологиях и сопровождались отчетами о результатах исследований и оценкой альтернативных устройств по методике Немецкой ассоциации газа и воды DVGW (технический протокол испытаний W512). Исследования были сосредоточены исключительно на предотвращении образования накипи. В этом тесте обработанная и необработанная жесткая вода проходят через электрический водонагреватель в течение 20 дней, а затем измеряется количество накипи, образовавшейся в нагревателе.
Рисунок 1. Устройства для оценки альтернативных устройств снижения образования накипи в соответствии с протоколом DVGW- 512.
Образующаяся накипь измеряется количественно и сравнивается с накипью, создаваемой необработанной водой в процентном соотношении. Для того чтобы устройство было сертифицировано DVGW образование накипи должно быть уменьшено на 80% и более. Испытываемые устройства включали:
Системы на основе каталитической кристаллизация NAC (TAC):
В качестве катализатора кристаллизации используются специальные поверхностно активные полимерные шарики в традиционном полимерном корпусе фильтра, которые создают каталитические центры для преобразования и роста микрокристаллов жесткости (кристаллы впоследствии высвобождаются с центров и остаются в растворе, не образуя накипи). Эта технология сертифицирована DVGW.
Электрически индуцированное осаждение.
Использует постоянный ток для образования мягкого осадка на электроде. Электрод требует периодической промывки для очистки.
Емкостная деионизация.
Ранее известная и усмовершенствованная технология, использующая постоянный ток для разделения ионов в воде на положительные и отрицательные виды с удерживанием их на угольных электродах. Технология позволяет снизить TDS и жесткость воды. Електроды регенерируются путем изменения полярности тока с периодической химической очисткой. Соответствует критериям сертификации DVGW по предотвращению образования накипи.
Электромагнитная обработка.
Устройства, как правило, состоят из провода, обвитого вокруг водопроводной трубы, через который пропускается ток высокой частоты. Индуцированное магнитное поле по заявлению производителей осаждает соли жесткости в виде кристаллов арагонита с формированием мягкой накипи (в отличие от кальцита, образующего твердую накипь). Точный механизм процесса не ясен, но предполагается, что определенную роль могут играть растворенные в воде кислород, кремний (силикаты) и карбонат-ионы.
Результаты промежуточных испытаний альтернативных технологий.
Результаты оценки бытовых систем водоподготовки, альтернативных ионообменному умягчению, были представлены доктором Питером Фоксом на саммите Аризонского отделения WQA. Перечислены устройства и общее снижение образования накипи, а также фотографии нагревательных элементов после испытания (вода с температурой 60оС).

Рисунок 2. Фото нагревательных элементов после испытания с применением альтернативных технологий умягчения.
Накипь, которую удалось измерить, показала содержание 87,2 процента карбоната кальция. Для расчета эффективности обработки результаты сравнивались с неочищенной водой (водопроводная вода Темпе (Аризона) из реки Солт Ривер со средней жесткостью 180 мг/л по CaCO3 (3,6 мг-экв/л). Нагреватели, используемые в исследовании, имели плотность энергии 25 Вт/см2, что ближе к фактической мощности электрического водонагревателя и отличается от требований протокола DVGW.
| Технология водоподготовки | Кристаллизация NAC | Электрически индуцированное осаждение | Электромагнитная обработка | Емкостная деионизация |
| Снижение накипи | 96,4% | 51,2% | 41,7% | 83,3% |
Таблица 2. Результаты испытаний.
Необходимот о отметить, что тестировалась только одна проблема жесткой воды – отложение накипи при нагревании. За исключением необработанной исходной воды вся образовавшаяся накипь была мягкой и сравнительно легко удалялась. В таблице 2 перечислены предполагаемые результаты оценки взаимодействия альтернативных технологий с другими проблемными проявлениями жесткой воды.
Итог.
Альтернативные устройства не являются умягчителями воды, так как не производят мягкую воду, обладающую низким солесодержанием или его полным отсутствием. Названия «квазиумягчения» или «кондиционирования» более приемлемы для характеристики таких систем водоподготовки, которые не умягчают воду, но эффективно препятствуют образованию накипи. Для многих промышленных и бытовых применений, предполагающих устранение проблемы образования накипи — это реальная альтернатива умягчителям. Скорее всего это альтернатива для потребителей, которых привлекают с одной стороны «зеленые технологии», с другой — отсутствие необходимости покупать, складировать и переносить мешки с солью. Однако, поверхность смесителя или стеклянная перегородка в ванной останутся с пятнами соли после испарения воды и, скорее всего, потребуют периодической очистки химическими средствами. К слову, мягкая вода после испарения также оставляет следы соды, удаление которых обычно не требует применения химических средств.
Источник информации:
- Fox, Peter, Evaluation of Alternatives to Domestic Ion Exchange Water Softeners, WRF-08-06, AWQA luncheon presentation November 19, 2010, referenced with permission.

