Іонний обмін. Основні процеси. Як змінюється склад води.
ПРОЦЕС 1. ПОМ’ЯКШЕННЯ.
Для видалення з води катіонів жорсткості застосовують сильнокислотну катіонообмінну смолу (катіоніт) у натрієвій формі. Регенерація здійснюється водним розчином NaCl (розчином таблетованої солі).
Пом’якшення не змінює солоність води, проте заміщає іони жорсткості на натрій, солі якого мають значно більшу пряму розчинність (зростання розчинності з підвищенням температури) і не утворюють накипний осад (зниження розчинності гідрокарбонатів в обсязі води при зростанні температури).
Те, як змінюється склад солей вихідної твердої води після пом’якшення:
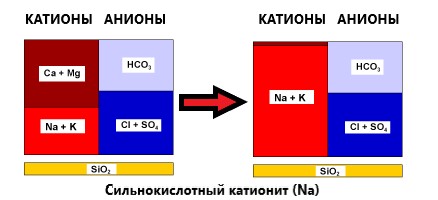
Загальний солевміст залишається незмінним. Кальцій та магній (іони жорсткості) обмінюються на натрій. У воді залишається незначна кількість кальцію та магнію, залишкова концентрація яких залежить від умов регенерації смоли.
P.S. Майже всі карбонати (солі вугільної кислоти із заміщенням двох іонів водню) – нерозчинні у воді солі вугільної кислоти. Усі гідрокарбонати (заміщений лише один іон водню, а не два) – розчинні у воді сполуки.
При нагріванні води, що містить надлишок розчиненого гідрокарбонату кальцію, виділяється вуглекислий газ і на стінках теплообмінника формується накип – осад нерозчинного карбонату кальцію. Чим вище загальна жорсткість і загальна лужність, тим більше накипу та вуглекислого газу виділяється в процесі нагрівання або випаровування.
Ca(HCO3)2 = CaCO3↓ + CO2 + H2O
Процес зберігає оборотність за зміни умов середовища.
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
ПРОЦЕС 2. ЗНИЖЕННЯ ЛУЖНОСТІ.
Процес іонного обміну, спрямований на вилучення карбонатної жорсткості, із застосуванням слабокислотної катіонообмінної смоли у водневій формі. Після обробки вода міститиме СО2. Регенерація слабокислотного катіоніту здійснюється водним розчином сильної кислоти, переважно соляної кислоти. Вуглекислий газ видаляється на стадії дегазації.
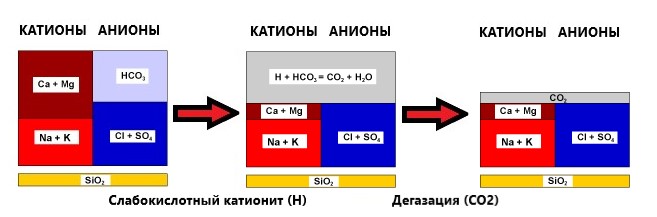
H++HCO3- → CO2 + H2O
Іони водню рекомбінуються з бікарбонат-аніоном вугільної кислоти, утворюючи воду і вуглекислий газ. Загальна солоність знижується – карбонатна жорсткість (катіони жорсткості + бікарбонат-аніони) повністю видаляється. Загальна жорсткість обробленої води = постійній (некарбонатній) жорсткості води.
ПРОЦЕС 3. КОМБІНАЦІЯ ПОМ’ЯКШЕННЯ ЗІ ЗНИЖЕННЯМ ЛУЖНОСТІ.
Процес іонного обміну, що характеризується послідовною обробкою води із застосуванням двох смол – слабокислотного катіоніту у водневій формі (видалення лужності) та сильнокислотного катіоніту у натрієвій формі (пом’якшення). Застосовність такого процесу може бути обумовлена тим, що загальна жорсткість значно перевищує загальну лужність. У разі рівності або у разі більш високої загальної лужності слабокислотний катіоніт у водневій формі виконає “цю роботу” самостійно. На першій стадії видаляється карбонатна (тимчасова) жорсткість, на другій – некарбонатна жорсткість.
Те, як змінюється склад води при послідовній обробці:
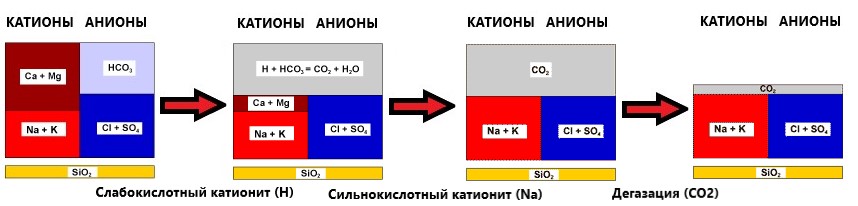
ПРОЦЕС 4. ДЕКАТІОНІЗАЦІЯ.
Видалення катіонів з води – процес, який досить рідко застосовується відокремлено. Найчастіше видалення катіонів – перша стадія процесу демінералізації. Регенерація сильнокислотного катіоніту (в Н-формі) здійснюється розчином сильної кислоти – HCl або H2SO4.
Те, як змінюється склад води в процесі декатіонізації із застосуванням сильнокислотного катіоніту в Н-формі:
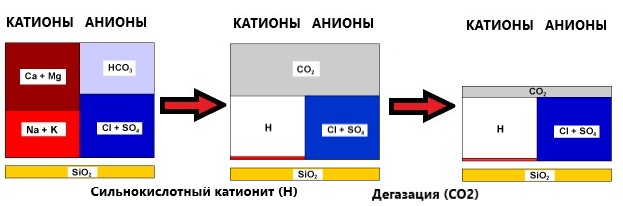
В результаті взаємодії виділяється вуглекислий газ (рекомбінація водню з бікарбонат-аніонами), видалення якого вимагає додаткової стадії дегазації. Солоність (мінералізація) води знижується. Загальна жорсткість = 0. Вода набуває кислої реакції (рН 2…5) і містить незначну “проскокову” концентрацію натрію (0,1…1 мг/л, залежно від умов регенерації).
ПРОЦЕС 5. ДЕМІНЕРАЛІЗАЦІЯ.
Багато технологічних завдань у промисловості, наприклад, які передбачають нагрівання води до утворення пари, вимагають застосування хімічно чистої води. Так як вода містить катіони та аніони завдання демінералізації (або, іншими словами, деіонізації) передбачає обробку води із застосуванням двох типів смол – катіонообмінної і аніонообмінної. Катіонообмінна смола у водневій формі регенерується розчином кислоти, аніонообмінна смола в OH-формі – розчином лугу. Якщо вихідна вода містить велику кількість гідрокарбонатів після катіонного обміну у воді утворюватиметься велика кількість вуглекислоти, що вимагає стадії дегазації (як мінімум, для видалення “додаткового навантаження” з сильноосновного аніоніту, що видаляє з води аніони ( з дуже низькою іонізацією) слабких кислот -SiO2 і CO2 ). Послідовність “катіоніт-дегазатор (опція)-аніоніт” обов’язкова, тому що якщо спочатку видаляти з води аніони, солі жорсткості будуть в лужному середовищі втрачати розчинність і осаджуватися в аніоніті у вигляді Ca(OH)2 або CaCO3.
Те, як змінюється склад води у процесі демінералізації:
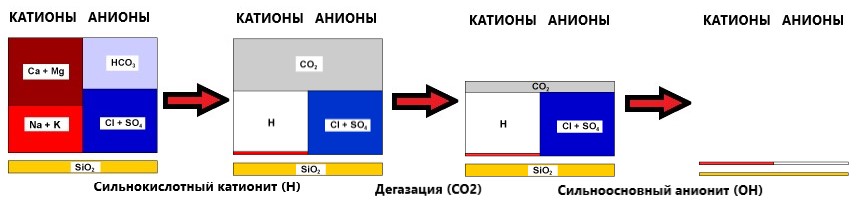
В результаті утворення на першій стадії водню і на другій стадії – гідроксильної групи замість катіонів і аніонів, що видаляються, утворюються нові молекули води. Оброблена вода практично не містить іонів, крім зневажливо малих залишкових концентрацій натрію та кремнію (найменша селективність з боку катіоніту до натрію та аніоніту до аніонів кремнієвих кислот).
ПРОЦЕС 6. ВИДАЛЕННЯ НІТРАТІВ.
Селективне видалення нітратів з води здійснюють із застосуванням нітрат-селективної сильноосновної аніонообмінної смоли у хлоридній формі, тобто, з регенерацією розчином NaCl. Регенерація здійснюється у протиточному режимі. Очікуваний проскок NO3 при протиточній регенерації 2…10 мг/л. Високий вміст у вихідній воді сульфатів (конкуруюча домішка) підвищує проскокову концентрацію NO3. Стандартна сильноосновна аніонообмінна смола в хлоридній формі має однакову селективність до сульфатів і нітратів.
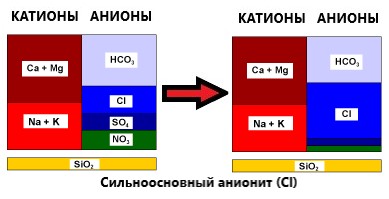
Видалення нітратів також можна здійснювати із застосуванням стандартної сильноосновної аніонообмінної смоли у хлоридній формі, але з паралельним видаленням сульфатів. Залежно від типу смоли (селективна або неселективна) сульфати частково видаляються (селективна) або повністю (неселективна). Бікарбонат-аніони видаляються частково і лише на початку “фільтроциклу”.

