Визначення жорсткості.
Сприйняття користувачами м’якої води часто виходить за рамки простого запобігання утворенню накипу. Вода, що містить двовалентні іони кальцію та магнію, залишає на контактних поверхнях твердий осад при нагріванні або випаровуванні. Ми називаємо таку воду жорсткою. Жорсткість може бути «тимчасовою», пов’язаною із аніонами слабких кислот (переважно з аніонами вугільної кислоти – гідрокарбонатами, рідше – силікатами або фосфатами) та постійною, пов’язаною із аніонами сильних кислот (сульфатами, хлоридами, нітратами). Назва тимчасова жорсткість отримала так, як її можна легко зменшити простим нагріванням води та перетворенням розчинної солі гідрокарбонату за реакцією:
Ca(HCO3)2 = CaCO3 + CO2 + H2O
Ця формула пояснює причину, через яку в бойлерах і посудомийних машинах утворюється накип і чому в промисловості для води, що живить котельне обладнання, задіяні процеси зниження лужності та пом’якшення, щоб зменшити як утворення накипу, так і виділення кислотної корозійно-агресивної пари, що містить CO2. Сам традиційний процес пом’якшення не знижує корозійну активність води, оскільки призводить до виділення агресивного CO2.
Аніонообмінне «пом’якшення» ( зниження лужності).
Зниження лужності дозволяє усунути накипоутворення без виділення CO2. Якщо оператор стикається з водою, лужність якої перевищує жорсткість, а корозійна активність є великою проблемою для водонагрівача, можна кондиціонувати воду, використовуючи аніонообмінну смолу (WBA або SBA), що регенерується хлоридом натрію. Цей процес призведе до заміни аніонів, включаючи гідрокарбонати, на хлориди. У результаті кип’ятіння води не призведе ні до утворення накипу, ні до виділення агресивного CO2. Отримані в результаті аніонного обміну хлориди кальцію та магнію – не солі жорсткості, накип не утворюють, в осад не випадають за жодних обставин.
Формування накипу.
Гідрокарбонати кальцію та магнію розчинні, але не існують у природі у вигляді сухих солей. При випаровуванні води навіть при температурі навколишнього середовища розчинені гідрокарбонати перетворюються на нерозчинні карбонати. Жорстка вода, залишена висихати, наприклад, коли розбризкувачі для газонів розпилюють воду на металевий паркан або автомобіль, утворює твердий накип, що важко видаляється. Тому на мийках або використовують знесолену воду, або вручну витирають воду з металевих і скляних поверхонь, щоб запобігти появі плям солі. Також вода, що випаровується з поверхні басейну, утворює твердий накип на лінії вододілу. Постійна жорсткість веде себе інакше і не така схильна до утворення накипу при нагріванні (проте гіпсовий накип (сульфат кальцію) може утворюватися якщо вода містить високі концентрації сульфатів). Гіпс може випадати в осад при концентруванні розчину з високим вмістом сульфату кальцію, наприклад, на поверхні мембрани зворотного осмосу. Сіль хлориду кальцію (CaCl2) краще розчиняється у воді порівняно із звичайною сіллю хлориду натрію. CaCl2 не випадає в осад ні за яких умов, але також не може залишатися довго в кристалічній формі (CaCl2 – гігроскопічна сіль, що вбирає вологу з атмосфери). З цієї причини цю сіль часто застосовують для посипання грунтових доріг, щоб зберігати невелику вологість поверхні та зв’язувати пил.
Якщо загальна лужність перевищує загальну жорсткість, вся жорсткість тимчасова. Якщо жорсткість перевищує лужність, є як тимчасова, так і постійна жорсткість. Як тимчасова, так і постійна жорсткість реагують з милом, утворюючи нерозчинний мильний шлак, який ми бачимо як кільцеве відкладення на межі вододілу по периметру ванни. Мило зазвичай це натрієва сіль жирних кислот і розчиняється у воді. Навпаки, двовалентні солі жорсткості погано розчинні. Мило діє як «іонообмінник», реагує з двовалентними іонами жорсткості , утворюючи осад. Щоразу, коли жорстка вода і мило змішуються, спочатку необхідно додати достатню кількість мила, щоб осадити всю жорсткість, а потім достатню кількість мила для виконання миючої дії. У душі мило та шампунь, здається, легше змиваються жорсткою водою. Але чи змиваються вони насправді? Ні! Вони осідають на шкірі у вигляді лужного залишку і стають причиною подразнення шкіри, сухості та ламкості волосся.
Крім того, багато засобів для чищення використовують лужні підсилювачі для підвищення pH, оскільки масла і бруд легше змиваються водою з більш високим pH. Однак більш високий pH також перетворює солі гідрокарбонату на солі карбонату, які потім випадають в осад. При ще вищому pH всі форми жорсткості втрачають розчинність і випадають в осад, створюючи ефект каламутної води. Це причина, через яку жорстка вода не може застосовуватися для регенерації аніонообмінної смоли в системах деіонізації, що регенеруються гідроксидом натрію. Побутові та промислові користувачі жорсткої води стикаються з додатковими витратами на заміну обладнання через накип або додатковими трудовитратами на усунення відкладень, обмеженням потоку через накип у трубах та додатковими енергетичними витратами на нагрівання води.
Можна узагальнити переваги використання м’якої води, просто перерахувавши недоліки використання жорсткої води:
– жорстка вода утворює осад у вигляді карбонатного накипу при нагріванні;
– жорсткість утворює осад при підвищеному рН;
– жорсткість утворює осад зі збільшенням концентрації (наприклад, зниження обсягу води внаслідок випаровування);
– твердий накип утворюється при простому випаровуванні жорсткої води;
– тверда вода реагує з милом, утворюючи нерозчинний мильний шлам.
Визначення м’якої води.
Пом’якшена вода не робить нічого з перерахованого вище. За визначенням WQA м’яка вода – це вода, яка містить жорсткість менше 0,34 мг-екв/л(<17,1 мг/л по CaCO3). Будь-який пристрій для кондиціонування води, що знижує жорсткість вихідної води до рівня менше 0,34 мг-екв/л, є пом’якшувачем. Будь-який пристрій для кондиціонування води, який не знижує жорсткість вихідної води до рівня нижче 0,34 мг-екв/л, відповідно, не може називатися пом’якшувачем, а вода, яку виробляє цей пристрій, не може називатися м’якою. Пристрій, який знижує жорсткість вихідної води, проте не до рівня нижче 0,34 мг-екв/л, також не може називатися пом’якшувачем. Не існує такого поняття, як частково пом’якшена вода, крім води, яку одержують шляхом змішування м’якої води з жорсткою.
Необхідні альтернативні технології.
Більшість пом’якшувачів води засновані на технології катіонного обміну і використовують сіль хлориду натрію (NaCl) як реагент. Сучасні пом’якшувачі мають високу ефективність, тобто. використовують найкраще співвідношення витрати солі до обсягу обробленої води. Також є пом’якшувачі, які використовують для регенерації хлорид калію (KCl) замість хлориду натрію (NaCl). Такі пом’якшувачі іноді називають «безсольовими» пом’якшувачами, проте KCl – це теж сіль.
Чи дійсно існують пристрої, які можна було б назвати безсольовими пом’якшувачами води? Так, є. Ми знаємо їх як дистилятори, системи зворотного осмосу та нанофільтрації, деіонізатори (іонний обмін), системи ємнісної деіонізації (EDI). На сьогоднішній день розвиток альтернативних технологій пом’якшення без регенерації сіллю отримав великий поштовх. Основною рушійною силою пошуку альтернатив іонообмінного пом’якшення стала необхідність у підтримці низького рівня солевмісту (TDS) стічних вод, щоб їх можна було повторно обробляти для скидання в грунтові води без необхідності знижувати TDS за допомогою доровартісного обладнання. Необхідність у низькому солевмісті стічних вод призвела до появи законів, що обмежують використання іонообмінних пом’якшувачів води, що регенеруються сіллю, у Каліфорнії, Аризоні, Техасі, Коннектикуті, Мічигані та Неваді.
Запобігання утворенню накипу.
Накип є найбільшою проблемою використання жорсткої води. На сьогоднішній день існує кілька технологій, спрямованих на зменшення утворення накипу. Перша і найбільш поширена технологія – видалення іонів, що спричиняють накип, за допомогою звичайного іонообмінного пом’якшувача з регенерацією сіллю. Існуютьситуації, коли з води разом із солями жорсткості необхідно видалити майже всі інші солі, і тоді застосовується технологія демінералізації. Також існують способи обробки води хімічними добавками, що або запобігають утворенню накипу, або роблять накип більш м’яким. Засоби для запобігання утворенню накипу працюють на принципі ізолювання солей жорсткості за допомогою хімічних добавок (хелатуючих речовин), які ефективно пов’язують іони металів, роблячи їх нереактивними. Приклад такої добавки – ЕДТА (етилендіамінтетраоцтова кислота, «Трилон Б»). Інші добавки (наприклад, низькі рівні поліфосфату) викликають утворення м’якого накипу, втручаючись у кристалічні решітку. Нарешті, існують пристрої фізичного очищення води, які не видаляють іони, що утворюють накип, та не додають у воду хімікати:
– пристрої, що запобігають відкладенню накипу (утворюють мікроскопічні кристали твердого накипу у водній фазі, які не дозволяють накипу відкладатися на поверхнях, блокувати потік та теплопередачу);
-пристрої, що запобігають утворенню твердого накипу, які перетворюють кальцит на арагоніт або якусь іншу форму м’якого накипу, що легше видаляється.
Всі вищезгадані технології продемонстрували різною мірою здатність зменшувати проблеми, пов’язані з накопиченням твердого накипу. У нашому списку з п’яти проблем із жорсткою водою, згаданих раніше, ці технології вирішують проблему №1 — утворення накипу.
Варіанти комерційної та промислової водопідготовки.
Якщо основною проблемою є запобігання утворенню накипу в котлі з подальшою втратою ефективності теплопередачі та витратами на технічне обслуговування, пов’язане з очищенням, більшість з перерахованих вище технологій знайдуть той чи інший рівень прийняття у споживача. Деякі з них приймаються з більшою готовністю, ніж інші. Наприклад, утворення м’якого накипу деякими фізичними технологіями водопідготовки все ще вимагатиме періодичних зупинок обладнання для очищення. Технології іонообмінного пом’якшення та демінералізації фактично видаляють іони жорсткості та виробляють воду, яка не утворює накипу.
Якщо Ви хочете отримати всі переваги м’якої води, вибір технологій стає значно коротшим. Реакційну здатність двовалентних катіонів жорсткості доведеться видалити з води одним з методів, перерахованих у таблиці 1. Потрібний результат можна отримати пом’якшенням або демінералізацією, або використовуючи для запобігання реакцій катіонів таку хімічну речовину як ЕДТА. У таблиці 1 показано ефективність різних технологій щодо різних негативних проявів жорсткої води.
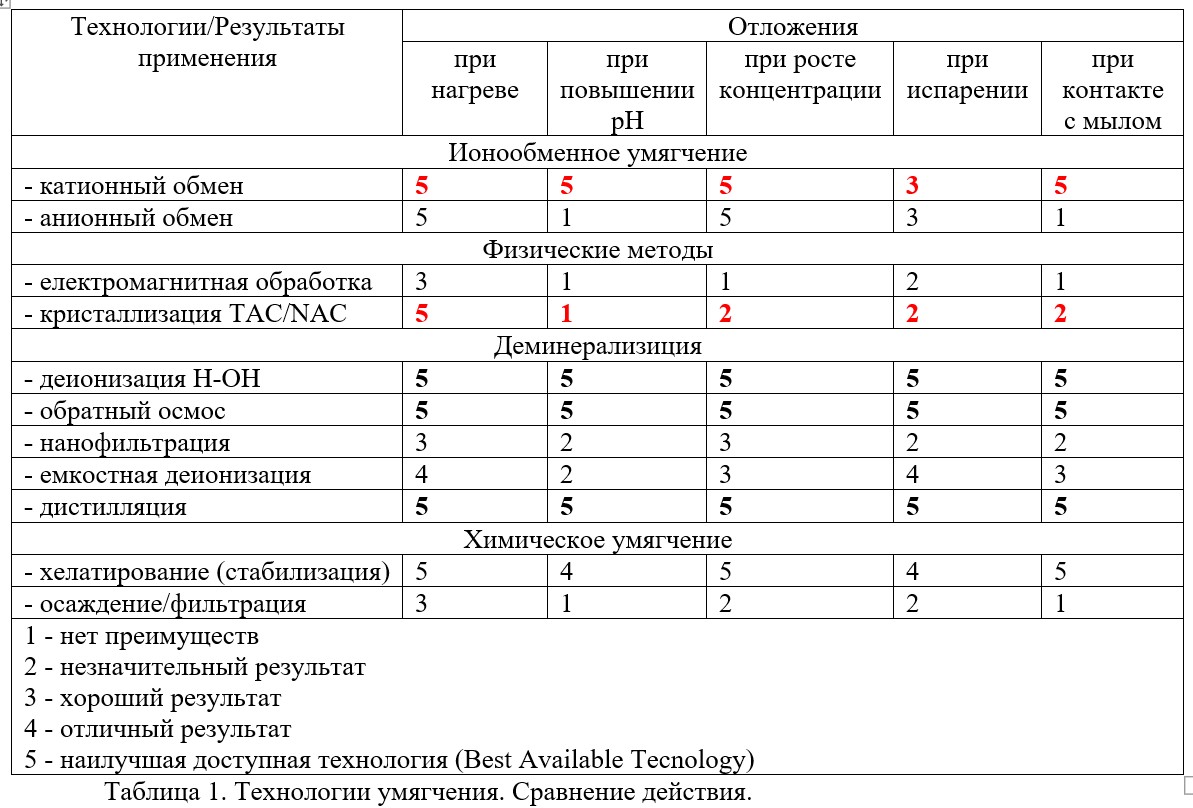
*катіонне або аніонне пом’якшення – відкладення на поверхнях після випаровування води (плями солі) не утворюють твердий або м’який накип, не містять солі жорсткості.
Обговорення таблиці 1.
Для прояву негативної дії у воді повинні бути присутні іони жорсткості у достатній кількості. Катіонообмінне пом’якшення, зворотний осмос, деіонізація та дистиляція – єдині процеси, які видаляють двовалентні іони практично до нуля.
Аніонний обмін видаляє протиіони (бікарбонати та сульфати). У результаті жорсткість не створює накип, але катіони кальцію і магнію, що залишилися в розчині, будуть реагувати з милом і осаджуватися при підвищеному pH (у вигляді гідроксидів кальцію і магнію).
Зворотний осмос (тільки при високому тиску) має практично 100% ефективність у відторгненні кальцію і магнію.
Нанофільтрація має нижчі показники відторгнення солей жорсткості. Ємнісні деіонізатори – відносно нові пристрої, які видаляють жорсткість за допомогою електричного тяжіння іонів до електродів за допомогою постійного струму та знижують утворення накипу приблизно до 95 відсотків. Однак залишкова жорсткість все ще дозволяє воді реагувати з милом і викликати сильне помутніння води при підвищенні pH. Хімічна хелатування по суті ізолює двовалентні іони так, щоб вони не могли вступати в реакції.Отримані хелати не утворюють накип при нагріванні або випаровуванні і не реагують з милом. Хімічний хелатуючий реагент (наприклад, ЕДТА) часто включається в склади миючих речовин спеціально для того, щоб дозволити милу виконувати свою роботу в жорсткій воді.
У меншій мірі ті хімічні добавки, що дозволяють накипу утворювати осад, але перешкоджають росту накипу, диспергуючи мікрочастинки, дозволяють великій кількості реактивної жорсткості залишатися в розчині. Поєднання дисперсного накипу та нового твердого накипу залишає на поверхні осад, який значно м’якше і легше видаляється. У розчині все ще міститься досить реактивної жорсткості реакції з милом або помутніння води при високому pH. Після застосування технології «холодного» вапнування (зниження жорсткості до 1…1.5мг-екв/л) зазвичай потрібне іонообмінне полірування для більшості застосувань. Технологія «гарячого» вапнування дозволяє знизити жорсткість до значення менше 0,34 мг-екв/л. Технологія вапнування через хімічну складність процесу та розмір обладнання не підходить ні для чого крім великих промислових або муніципальних застосувань.
Фізичні технології пом’якшення води поділяються на дві групи.
Перша група:
– технології запобігання утворенню накипу, що працює на принципі стимуляції утворення накипу попередньо до надходження води у водонагрівач. Ця група включає технологію каталітичної кристалізації NAC (TAC), яка каталізує утворення у воді субмікронних кристалів (кристали залишаються у потоці воді у вигляді колоїдно-зважених частинок, які не прилипають до нагрітих поверхонь);
– технології електрично індукованого осадження, що утворює м’який накип на електроді (необхідне періодичне очищення).
Друга група:
– технології запобігання утворенню накипу, що змінюють склад води. До цієї групи відноситься ємнісна деіонізація (яка фактично знижує солевміст води, притягуючи розчинні іони до селективних електродів) і електромагнітні пристрої, які, як стверджують виробники, утворюють м’який осад, що складається з аморфних кристалів арагоніту і ватериту замість стійкішої твердої форми накипу, з кристалів кальциту.
На саміті Арізонського відділення WQA у листопаді 2010 року професор інженерної екології Університету Арізони доктор Пітер Фокс (Темпе, Арізона) виконав доповідь(1) із проміжними результатами досліджень альтернативних пристроії для очищення води. Зокрема, його дослідження є оцінкою альтернатив регенерованим побутовим пом’якшувачам води. Вибрані для дослідження пристрої були засновані на різних технологіях та супроводжувалися звітами про результати досліджень та оцінкою альтернативних пристроїв за методикою Німецької асоціації газу та води DVGW (технічний протокол випробувань W512). Дослідження були зосереджені виключно на запобіганні утворенню накипу. У цьому тесті оброблена і необроблена жорстка вода проходять через електричний водонагрівач протягом 20 днів, а потім вимірюється кількість накипу, що утворився в нагрівачі.
Рисунок 1. Пристрої для оцінки альтернативних пристроїв зниження освіти накипу відповідно до протоколу DVGW- 512.
Накип, що утворюється, вимірюється кількісно і порівнюється з накипом, що створюється необробленою водою у відсотковому співвідношенні. Для того, щоб пристрій було сертифіковано DVGW, відкладення накипу повинне бути зменшене на 80% і більше. Використовувані пристрої включали:
Системи на основі каталітичної кристалізації NAC (TAC):
Як каталізатор кристалізації використовуються спеціальні поверхнево активні полімерні кульки в традиційному полімерному корпусі фільтра, які створюють каталітичні центри для перетворення і зростання мікрокристалів жорсткості (кристали згодом вивільняються з центрів і залишаються в розчині, не утворюючи накипу). Ця технологія сертифікована DVGW.
Електрично індуковане осадження.
Використовує постійний струм для утворення м’якого осаду на електроді. Електрод вимагає періодичного промивання для очищення поверхні.
Ємнісна деіонізація.
Раніше відома та удосконалена технологія, що використовує постійний струм для поділу іонів у воді на позитивні та негативні з утримуванням їх на вугільних електродах. Технологія дозволяє знизити TDS та жорсткість води. Електроди регенеруються шляхом зміни полярності струму з періодичним хімічним очищенням. Відповідає критеріям сертифікації DVGW щодо запобігання утворенню накипу.
Електромагнітна обробка.
Пристрої, як правило, складаються з дроту, обвитого навколо водопровідної труби, через який пропускається струм високої частоти. Індуковане магнітне поле за заявою виробників змінює тип осаду солей жорсткості у вигляді кристалів арагоніту з формуванням м’якого накипу (на відміну від кальциту, що утворює твердий накип). Точний механізм процесу не зрозумілий, але передбачається, що певну роль можуть грати розчинені у воді кисень, кремній (силікати) та карбонат-іони.
Результати проміжних випробувань альтернативних технологій.
Результати оцінки побутових систем водопідготовки, альтернативних іонообмінному пом’якшенню, були представлені доктором Пітером Фоксом на саміті Арізонського відділення WQA. Перераховані пристрої та загальне зниження утворення накипу, а також фотографії нагрівальних елементів після випробування (вода з температурою 60оС).

Рисунок 2. Фото нагрівальних елементів після випробування із застосуванням альтернативних технологій пом’якшення.
Накип, який вдалося виміряти, показав вміст 87,2 відсотка карбонату кальцію. Для розрахунку ефективності обробки результати порівнювалися з неочищеною водою (водопровідна вода Темпе (Арізона) із річки Солт Рівер із середньою жорсткістю 180 мг/л по CaCO3 (3,6 мг-екв/л). Нагрівачі, що використовуються в дослідженні, генерували теплову енергію щільністю 25 Вт/см2, що ближче до фактичної потужності електричного водонагрівача та відрізняється від вимог протоколу DVGW.
| Технологія водопідготовки | Кристалізація NAC | Електрично індуковане осадження | Електромагнітна обробка | Ємнісна деіонизація |
| Зниження накипу | 96,4% | 51,2% | 41,7% | 83,3% |
Таблиця 2. Результати випробувань.
Необхідно відзначити, що тестувалася тільки одна проблема жорсткої води – відкладення накипу при нагріванні.За винятком необробленої вихідної води весь накип, що утворився, був м’яким і порівняно легко видалявся. У таблиці 2 наведено передбачувані результати оцінки взаємодії альтернативних технологій з іншими проблемними проявами жорсткої води.
Висновки.
Альтернативні пристрої не є пом’якшувачами води, тому що не виробляють м’яку воду, що має низький вміст солевмісту або його повною відсутністю. Назви «квазіпом’якшення» або «кондиціювання» більш прийнятні для характеристики таких систем водопідготовки, які не пом’якшують воду, але ефективно перешкоджають утворенню накипу. Для багатьох промислових та побутових застосувань, що передбачають усунення проблеми утворення накипу – це реальна альтернатива пом’якшувачам. Швидше за все це альтернатива для споживачів, яких залучають з одного боку «зелені технології», з іншого – відсутність необхідності купувати, складувати та переносити мішки із сіллю. Однак, поверхня змішувача або скляна перегородка у ванній залишаться з плямами солі після випаровування води і, швидше за все, вимагатимуть періодичного очищення хімічними засобами. До речі, м’яка вода після випаровування також залишає сліди соди, видалення яких зазвичай не потребує застосування хімічних засобів.
Джерела інформації:
- Fox, Peter, Evaluation of Alternatives to Domestic Ion Exchange Water Softeners, WRF-08-06, AWQA luncheon presentation November 19, 2010, referenced with permission.

