![]() До появи сучасних іонообмінних процесів єдиним способом отримання чистої води була дистиляція. Всупереч поширеній думці одноступенева дистиляція не дозволяє отримати хімічно чисту воду. Фактично, для досягнення чистоти води, отриманої при іонному обміні в процесі деіонізації, потрібно більше 20 послідовних дистиляцій з використанням інертних кварцових посудин.
До появи сучасних іонообмінних процесів єдиним способом отримання чистої води була дистиляція. Всупереч поширеній думці одноступенева дистиляція не дозволяє отримати хімічно чисту воду. Фактично, для досягнення чистоти води, отриманої при іонному обміні в процесі деіонізації, потрібно більше 20 послідовних дистиляцій з використанням інертних кварцових посудин.
Загальні положення.
- Видалення всіх домішок з води та отримання високоякісної води називається процесом деіонізації (DI).
- Деіонізовану воду можна отримати різними методами, але в цій статті ми розглядаємо лише метод іонного обміну.
- У процесі іонного обміну застосовуються катіонообмінні та аніонообмінні смоли, електростатично пов’язані з іонами водню та гідроксильної групи відповідно.
- Смола змішаної дії поєднує катіонообмінну та аніонообмінну смоли у певному співвідношенні.
- Смола змішаної дії ефективніша ніж двошарові або двостадійні системи деіонізації.
- Смола змішаної дії з часом виснажується, потребує регенерації або заміни.
- Іонообмінна система (“іонообмінник”) зі смолою змішаної дії може використовуватися для отримання води високої якості з водопровідної води (в т.ч. у резервних процесах), проте через високу концентрацію катіонів та аніонів у водопровідній воді фільтр змішаної дії швидко вичерпає свою ємність.
- Зазвичай система зі смолою змішаної дії – останній етап у технологічному “ланцюжку” отримання надчистої води. Система зі смолою змішаної дії встановлюється після двостадійного іонообмінного демінералізатора або після системи зворотного осмосу. При такому застосуванні іонообміна система змішаної дії забезпечує додаткове очищення («полірування») раніше демінералізованої води та здатна продукувати вже надчисту воду з питомим опором до 18,2 мОм х см (при цьому зберігаючи високу продуктивність та термін служби протягом кількох місяців при правильному проектуванні).
- При використанні «іонообмінника» змішаної дії із системою зворотного осмосу продуктивність може істотно знижуватися через поглинання пермеатом атмосферного CO2. Цей CO2 не відображається контролером електропровідності зворотного осмосу, але видаляється аніонообмінною смолою, скорочуючи загальний термін служби змішаної смоли.
- Контроль вичерпання робочої ємності «іонообмінника» змішаної дії може здійснюватися простим вбудованим вимірювачем опору.
- При вичерпанні ємності заміна смоли змішаної дії – найбільш логічне та просте рішення, яке не потребує організації складного процесу регенерації.
- Фільтри змішаної дії – відмінний спосіб видалити залишковий солевміст і реактивний кремній з води після системи зворотного осмосу (на відміну від колоїдного кремнію реактивний кремній не видаляється механічною фільтрацією).
- У робочому циклі вода надходить у корпус зі змішаною смолою через верхній дистриб’ютор у напрямку зверху-вниз.
- Смола змішаної дії дозволяє отримати надчисту воду, проте процес регенерації може бути занадто складним. До початку регенерації смоли необхідно гідравлічно розділити на два окремих шари (катіоніт і аніоніту) протиточним промиванням за рахунок різної щільності. Регенерація вимагає великої кількості реагентів (кислота та луг) та складної організації циклів. Тому смоли змішаної дії зазвичай застосовуються для полірування попередньо демінералізованої води до рівня електропровідності води1 мкСм/см і нижче та замінюються без регенерації.
 Іонний обмін. Процеси.
Іонний обмін. Процеси.
Створення полімеру з назвою «стирол-дивінілбензол» проклало шлях до створення сучасних сильноосновних аніонообмінних (SBA) і сильнокислотних катіонообмінних (SAC) смол , що застосовуються в іонообмінних процесах. Процес іонного обміну легко візуалізувати. Шар з нерозчинних полімерних кульок смоли, що містять активні центри (функціональні групи) з обмінними іонами, поміщається в корпус, через який протікає потік води. Іони з води вибірково притягуються до активних центрів смоли, обмінюючись з іонами, пов’язаними з активним центром. Цей процес створює новий склад води з іншими хімічними властивостями. Приклад такої зміни складу – процес пом’якшення із застосуванням сильнокислотного катіоніту у натрієвій формі (з обмінним натрієм в активному центрі).  В ході процесу пом’якшення катіони кальцію і магнію замінюються на катіони натрію, який усуває проблему накипоутворення і розглядається як більш прийнятний іон для багатьох застосувань води. Однак, якщо пом’якшена вода буде використана для живлення парового котла, гідрокарбонати натрію у складі пом’якшеної води при перегріванні та утворенні пари будуть руйнуватися з виділенням агресивного вуглекислого газу. Для усунення цієї проблеми з води потрібно видалити лужність і створити інший склад води в процесі іонного обміну – замінити аніони гідрокарбонату на аніони хлориду. Хлориди не випаровуються та не виділяють вуглекислий газ.
В ході процесу пом’якшення катіони кальцію і магнію замінюються на катіони натрію, який усуває проблему накипоутворення і розглядається як більш прийнятний іон для багатьох застосувань води. Однак, якщо пом’якшена вода буде використана для живлення парового котла, гідрокарбонати натрію у складі пом’якшеної води при перегріванні та утворенні пари будуть руйнуватися з виділенням агресивного вуглекислого газу. Для усунення цієї проблеми з води потрібно видалити лужність і створити інший склад води в процесі іонного обміну – замінити аніони гідрокарбонату на аніони хлориду. Хлориди не випаровуються та не виділяють вуглекислий газ.  Іонообмінний процес зниження лужності здійснюється із застосуванням сильноосновного аніоніту II типу в хлоридній формі (з обмінним хлоридом в активному центрі).
Іонообмінний процес зниження лужності здійснюється із застосуванням сильноосновного аніоніту II типу в хлоридній формі (з обмінним хлоридом в активному центрі).
Іонообмінна деіонізація (DI) – це двоетапний процес, при якому задіюється послідовно два шари: перший шар катіоніту (з обмінним воднем H+) і другий шар аніоніту (з обмінною гідроксильною групою OH-). Перша реакція в шарі катіоніту замінює всі катіони на іон водню і перетворює всі аніони на кислоти.  Друга реакція у шарі аніоніту заміщає всі аніони кислот, включаючи силікати SiO2, на гідроксильну групу та нейтралізує воду. Кінцевий продукт – вода.
Друга реакція у шарі аніоніту заміщає всі аніони кислот, включаючи силікати SiO2, на гідроксильну групу та нейтралізує воду. Кінцевий продукт – вода. 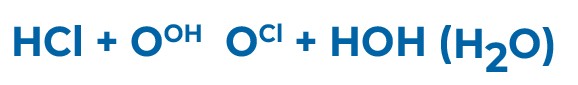 Логічно припустити, що деіонізації з двох шарів можна було б замінити їх точною сумішшю в так званому змішаному шарі (англійська назва – mixed bed). У 1949 році вперше використали змішані шари та отримали воду високої якості. Єдиним, але украй незручним недоліком стало те, що для регенерації смол їх доводилося ретельно поділяти. Тому двошарова концепція послідовної деіонізації у двох окремих корпусах залишилася більш практичною, зручною та менш витратною – для регенерації смоли не потрібно було витягувати з корпусів та розділяти. Застосування тришарової деіонізації (катіоніт-аніоніт-катіоніт) дозволяло без змішування шарів отримати ще чистішу воду з питомим електричним опором 1 мОм х см.
Логічно припустити, що деіонізації з двох шарів можна було б замінити їх точною сумішшю в так званому змішаному шарі (англійська назва – mixed bed). У 1949 році вперше використали змішані шари та отримали воду високої якості. Єдиним, але украй незручним недоліком стало те, що для регенерації смол їх доводилося ретельно поділяти. Тому двошарова концепція послідовної деіонізації у двох окремих корпусах залишилася більш практичною, зручною та менш витратною – для регенерації смоли не потрібно було витягувати з корпусів та розділяти. Застосування тришарової деіонізації (катіоніт-аніоніт-катіоніт) дозволяло без змішування шарів отримати ще чистішу воду з питомим електричним опором 1 мОм х см.
Іонний обмін. Реакція рівноваги.
Іонний обмін – це реакція рівноваги. Якщо кінцевий продукт декатіонування вода з кислотою і кислота використовується для регенерації, то катіоніт буде відчувати деяке збільшення навантаження в міру збільшення загального солевмісту (TDS) у вихідній воді. Чим вище TDS, тим більше кислоти в кінцевому продукті (обробленої в шарі катіоніту воді) і тим нижче pH. У певний момент pH води може стати досить низьким, щоб розпочати регенерацію катіоніту, що призведе до витіснення раніше обміняних катіонів, переважно натрію. Витіснений натрій перетвориться в наступному шарі аніонообмінної смоли на гідроксид натрію, що призведе до зростання рН (більше 10) і обмежить застосування цієї води. Якщо ми подивимося на рівняння співвідношення натрію/водню для катіонного обміну, то легко побачимо, що відбувається: 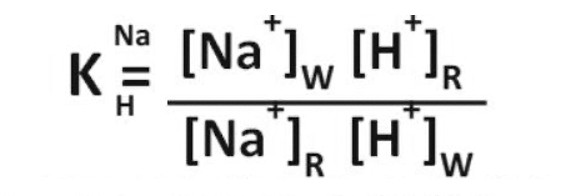 Це рівняння показує, що співвідношення для катіонообмінної смоли у формі H+ буде залежати від концентрації натрію у воді [Na+]W та концентрації водню на смолі [H+]R. Таким чином, чим вище солевміст води і чим краща регенерація, тим більша ця рівновага зміщується вправо. У міру виснаження ємності шару і, одночасно, підвищення концентрації натрію на смолі і концентрації водню у воді, значення в нижній частині рівняння збільшуються, і рівновага зміщується вліво – настає межа, після якого витік натрію збільшується.
Це рівняння показує, що співвідношення для катіонообмінної смоли у формі H+ буде залежати від концентрації натрію у воді [Na+]W та концентрації водню на смолі [H+]R. Таким чином, чим вище солевміст води і чим краща регенерація, тим більша ця рівновага зміщується вправо. У міру виснаження ємності шару і, одночасно, підвищення концентрації натрію на смолі і концентрації водню у воді, значення в нижній частині рівняння збільшуються, і рівновага зміщується вліво – настає межа, після якого витік натрію збільшується.
Вода високого ступеня чистоти без змішаних шарів.
У міру того, як pH очищеної води (як з катіонообмінного, так і з аніонообмінного шару) відхиляється від значення 7, реакція рівноваги уповільнюється і перешкоджає перебігу іонообмінної реакції. Отже, зі збільшенням загального солевмісту (TDS) збільшується витік натрію. У міру збільшення витоку натрію збільшується і pH аніонного продукту, що, своєю чергою, збільшує виток SiO2. При відхиленні pH обох продуктів від значення 7 двоступенева система DI буде обмежена за загальним вмістом солі (TDS). Досвід підказує, що ця межа TDS становитиме близько 2000 мг/л. Однак установка двох або більше двоступінчастих систем поспіль вирішить цю проблему. Загалом катіонообмінний шар системи DI знижує вміст катіонів у воді на 99,5%. Це означає, що при подачі води з вмістом солі 1000 мг/л буде спостерігатися витік натрію близько 5 ppm. При русі через аніоніт натрій перетворюється на гідроксид натрію та результуючий pH складе близько 10, а питомий опір оброблення води – близько 60 кОм. Цього може виявитися достатнім для автомийки, але не більше. Однак, якщо цю очищену воду подати на інший катіоніт, зниження pH до 7 буде дуже сприятливим. Якщо ми побачимо додаткове зниження вмісту катіонів на 99%, то на виході з «повторного» шару катіоніту концентрація натрію становитиме менше 0,1 мг/л. Одного цього достатньо, щоб збільшити питомий опір води майже до 1 мОм х см. Додайте ще один аніоніт і опір понад 1 мОм х см можна буде досягти навіть без використання змішаного шару зі складним процесом регенерації.
Система деіонізації зі смолою змішаного типу.
Ідея кількох послідовних циклів деіонізації призвела до розробки системи змішаного типу. Якщо два цикли катіонування здатні підняти питомий опір з 60кОм х см до 1 мОм х см, то на що потенційно здатні кілька десятків циклів катіонування/аніонування? Відповідь – ми можемо отримати очищену воду з питомим опором більше 18,2 мОм х см. Виміряти питомий опір води, що перевищує це значення, практично неможливо, оскільки надчиста вода стає автоіонною, починає іонізуватися, перетворюючись на струмопровідну речовину. У літературі зазначено, що максимальний питомий опір для надчистої води становить 18,2 мОм х см. Значення TDS, що відповідає цьому питомому опору, становить менше 0,03 ppm. Навіть погано регенерований змішаний шар може виробляти воду з питомим опором близько 10 мОм х см.
Співвідношення катіоніту та аніоніту.
Реакція іонного обміну протікає у розбавлених розчинах. У міру проходження вихідної води через змішаний шар (mixed bad) та заміщення заряджених іонів водою, загальний солевміст (TDS) знижується, і реакція успішно завершується. Таким чином, робоча ємність змішаної смоли може бути дуже близька до загальної ємності відповідних смол катіоніту та аніоніту у двошаровій системі. У двошаровій системі співвідношення ємності SAC та SBA становить приблизно 2:1. Однак у змішаному шарі співвідношення ближче до абсолютної загальної ємності 1,95:1,2. Оскільки ємність катіоніту на 50% вище, ніж аніоніту, ми компенсуємо це співвідношення, створюючи змішаний шар з 60% аніоніту і 40% катіоніту. Ця пропорція забезпечує невелику перевагу в ємності по катіонів і запобігає забрудненню аніоніту солями жорсткості. Перевага змішаного шару полягає не тільки в одержанні води більш високого ступеня чистоти, але й у більшій продуктивності порівняно з двостадійною системою DI. У змішаному шарі вода, що обробляється, багаторазово «полірується» за допомогою безперервних і одночасних реакцій іонного обміну катіонів і аніонів, що призводить до отримання води з дуже низькою електропровідністю до 0,05 мкСм/см (високим питомим опором до 18,2 мОм х см). Системи деіонізації зі змішаним шаром традиційно застосовуються як наступна стадія «полірування» демінералізованої води внаслідок іншого процесу демінералізації – зворотного осмосу, двостадійної іонообмінної демінералізації чи дистилювання. Потреба надчистої води актуальна в енергетиці, у виробництві напівпровідникової електроніки або фармацевтичних препаратів. Подвійна природа смоли змішаної дії дозволяє їй досягати рівнів видалення іонів, що значно перевершують можливості окремих катіонних та аніонних шарів.
Смола змішаної дії. Регенерація.
Після вичерпання обмінної ємності смола змішаної дії може бути регенерованою. До початку регенерації протиточним промиванням гідравлічно розділяють змішану смолу за рахунок різної щільності на два окремих шари – катіоніт та аніоніт. Розчин кауcтической соди (гідрооксиду натрію NaOH) подають знизу в шар аніонообмінної смоли, розчин соляної кислоти (HCl) одночасно подають зверху в шар катіонообмінної смоли. Скидання відпрацьованих розчинів здійснюється одночасно через загальний колектор. 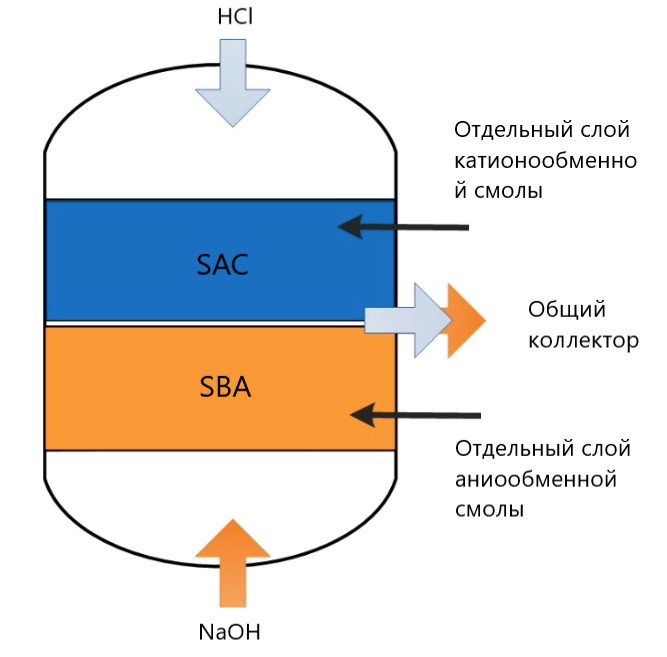 Після регенерації шарів послідовно запускаються цикли: повільного промивання чистою водою для витіснення залишків кислоти та лугу, дренажу (видалення води з шарів перед подачею повітря), перемішування стисненим повітрям, заповнення водою корпусу та прямоточного промивання.
Після регенерації шарів послідовно запускаються цикли: повільного промивання чистою водою для витіснення залишків кислоти та лугу, дренажу (видалення води з шарів перед подачею повітря), перемішування стисненим повітрям, заповнення водою корпусу та прямоточного промивання.

