Безнапірна аерація створює передумови видалення заліза з анаеробної води свердловини у концентраціях до 10 мг/л в найбільш економний спосіб.
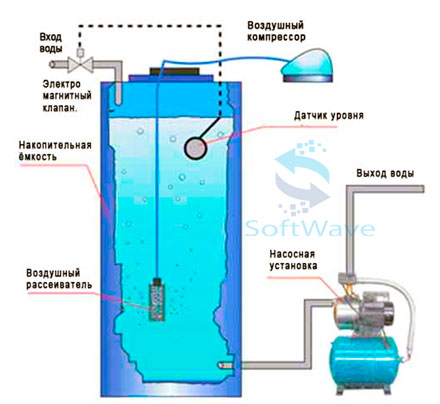
Форсунки розпорошують воду у повітрі у відкриту контактну ємність. Контакт води з атмосферним повітрям порушує вихідну рівновагу анаеробної підземної води та призводить до формування нового урівноваженого стану. Вуглекислота та сірководень втрачають розчинність і залишають воду, натомість вода поглинає атмосферний кисень. Різниця парціальних тисків на межі розділу фаз визначає швидкість та напрямок дифузії газів з води в повітря і навпаки. Усі масообмінні процеси — у точній відповідності до закону Генрі-Дальтона. З втратою вуглекислоти та сірководню зростає показник рН. Насичення води киснем зумовлює зростання окисного потенціалу середовища. Збільшення водневого показника призводить до дестабілізації сполук двовалентного заліза. Кисень окислює залізо. Швидкість окиснення двовалентного заліза визначається водневим показником – збільшення рН на 1 одиницю збільшує швидкість окиснення приблизно 10 раз!
Залізо прагне досягти найвищої форми валентності, набути термодинамічно стійкого стану, окислившись до кінцевого продукту – гідроксиду заліза.
Справа залишиться за малим — видалити нерозчинні частки гідроксиду фільтруванням води в напірному фільтрі.
Тепер докладніше, з акцентом на окремих аспектах!
Вода може містити залізо у двох формах окислення (Fe2+, Fe3+), у складі комплексних сполук або у вільному стані.
Свердловина вода містить переважно розчинене залізо у двовалентній формі та інші метали в низькій валентності, не містить кисень, містить вуглекислоту і сірководень, має, як правило, слабокислу реакцію (низький рН), і являє собою відновне середовище (окислювально-відновний потенціал Еh< 0). Отже, дія установок знезалізнення має бути зосереджено на видаленні саме такої двовалентної форми заліза у воді з перерахованими характеристиками та властивостями.
Кисень, час контакту та площа поверхні контакту!
Безнапірна аерація передбачає використання кисню з атмосферного повітря, як окислювача. Низький окисний потенціал кисню обумовлює необхідність достатнього часу експозиції – часу на дифузію кисню та стабілізацію стану окислених форм. Більше заліза – більший час експозиції. Вода з концентрацією заліза 5 мг/л вимагатиме для окислення експозиції не менше 15-20 хвилин. Крім концентрації заліза час окиснення прямо визначатиметься площею поверхні контакту води та повітря.
Взаємодія у відкритій контактній ємності 1 кубічного метра води з повітрям лише через дзеркало води забезпечить контактну площу поверхні розділу фаз 0,5-2м2. Цієї площі контакту замало.
Розпилення 1 кубічного метра води через аераційні форсунки в повітряному просторі відкритої контактної ємності в безнапірному варіанті аерації забезпечить поверхню контакту близько 40-70 м2. Це вже значно краще.
Наявність повітряного компресора та ефективний барботаж у контактній ємності дозволить збільшити площу поверхні контакту до 80-150 м2.
Застосування статичного міксера, заповненого кільцями Рашига або насадками Паля, може забезпечити поверхню розділу фаз для кубічного метра води площею близько 400-500м2. Усі результати пізнаються у порівнянні.
Окислювальний потенціал кисню! Атмосферний кисень чи озон?
З усіх традиційних окислювачів, що застосовуються у водопідготовці, атмосферний кисень О2 має найнижчий окисний потенціал (+0,41В), озон О3 – найвищий потенціал (+2,07В).
Озон має найбільшу «окислювальну силу» і реагує фактично з будь-якою речовиною, здатною окислюватися. Кисень такої сили не має. Кисень не окислює всі здатні до окислення речовини. Кисень окислює речовини вибірково. Кисень не забезпечує дезинфекцію води. Слабкий окисний потенціал кисню не дозволяє окислити органічне залізо.
Але кисень добре окислює двовалентне залізо і не створює небажані побічні продукти, властиві дії інших, сильніших окислювачів (хлору, озону). Чи не у слабких взаємодіях криється справжня сила тонких природних процесів окиснення та фільтрації води у гірських джерелах? Кисень залишається слабким, але при цьому єдиним по-справжньому екологічно чистим окислювачем у сучасній водопідготовці. Чистим та безкоштовним!
Звичайно ж, вибір окислювача має враховувати форми заліза у водізі свердловини.


